このページで
免疫グロブリンFc受容体(FcR)は、様々な造血細胞によって発現される膜結合タンパク質であり、異なる免疫グロブリンクラスおよびサブクラスのFc領域を特異的に認識して結合します。これらには、IgGに対するFcγRI/CD64、FcγRII/CD32、およびFcγRIII/CD16、IgEに対するFcεRI、IgAに対するFcαRI/CD89、IgMに対するFcµR、そしてIgAとIgMの両方に対するFcα/µRが含まれます。さらに、腸管上皮細胞、胎盤、および内皮に存在する新生児Fc受容体(FcRn)、B細胞およびマクロファージ上の低親和性FcεRII/CD23、粘膜上皮細胞上のポリマーIg受容体(pIgR)など、異なる細胞型上の他の受容体もIg分子と相互作用します。
抗体の有効性は、抗原エピトープを認識する能力と、それぞれのFc受容体に結合することを可能にする固有の柔軟性に左右されます。白血球上のFc受容体が活性化されると、炎症誘発作用、抗炎症作用、免疫調節作用など、一連の免疫応答が誘発されます。しかし、マウスとヒトのFcγ受容体はそれぞれ異なり、その発現パターンも異なるため、前臨床モデルにおける治療用抗体の薬力学的(PD)特性を評価することは困難です。
当社は、ヒトFcRのin vivo機能研究のためのFcRヒト化マウスモデルを開発しました。これらのモデルでは、対応する内因性マウスFcR遺伝子が欠損しており、ヒトFcR遺伝子の発現パターンを正確に再現するヒトFcR遺伝子が発現しています。FcR遺伝子ヒト化マウスを用いて、様々な細胞傷害性抗体や治療用抗体のin vivo活性を評価することで、ヒト免疫グロブリンFc領域のエフェクター機能に関する重要な知見が得られました。当社は、これらのモデルを提供することで、悪性腫瘍、自己免疫疾患、炎症性疾患、感染症を標的とした治療用ヒト抗体の評価における重要な前臨床リソースとしての地位を確立しました。
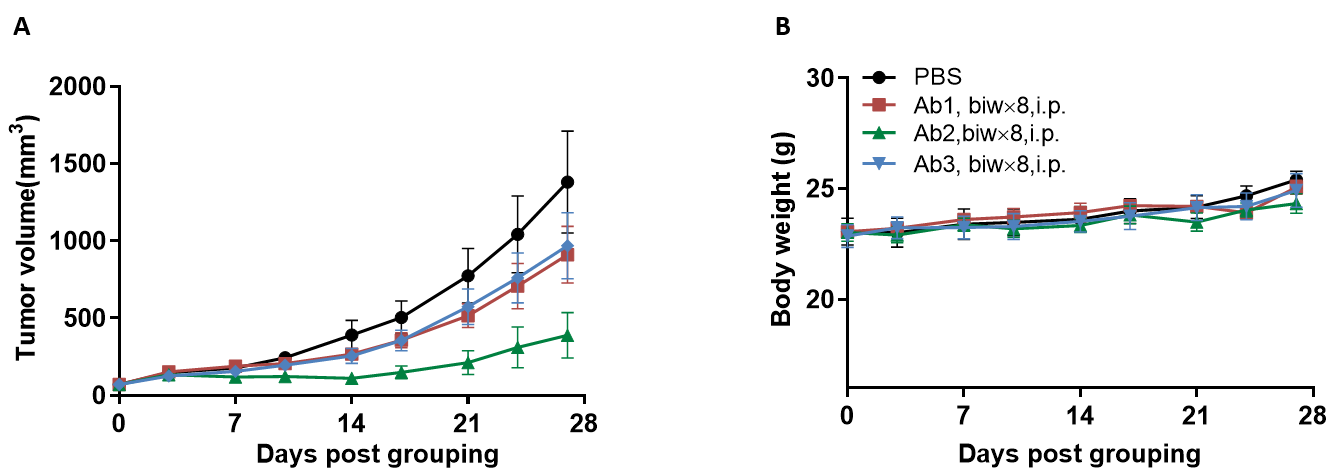
B-hCD16AマウスにおけるヒトCD16A抗体の抗腫瘍活性
(A)ヒトCD16A抗体はB-hCD16AマウスにおいてMC38腫瘍の成長を阻害しました。MC38結腸癌細胞を皮下に移植したB-hCD16Aマウス(13週齢、雌、n=7)に、腫瘍体積が約70mm³に達したときにグループ分けし、B図に示された用量とスケジュールに従ってヒトCD16A抗体を投与しました。(B)投与中の体重の変化。A図に示すように、抗ヒトCD16A抗体は、B-hCD16Aマウスにおける腫瘍増殖の抑制に有効であり、B-hCD16Aマウスが、抗ヒトCD16A抗体評価の強力な前臨床モデルであることを示しました。値は平均±SEMで示されます。
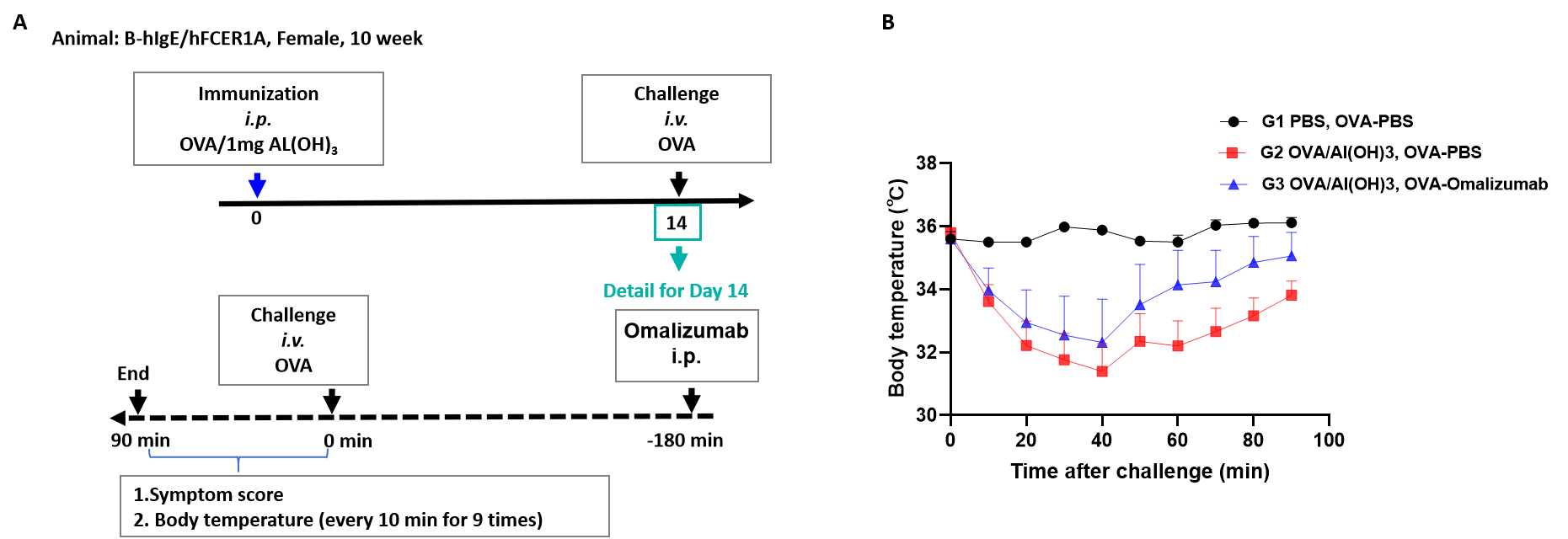
OVA誘導のASAに対するOmalizumabの有効性 B-hIgE/hFCER1Aマウス(H/H、H/H)にOVA/Al(OH)3免疫を0日目に施し、14日目にOVAを投与しました。14日目の投与3時間前にOmalizumab(in house)を投与しました。(A)投与後0分から90分までマウスの体温を記録しました。(B)ASAモデルにおいて、Omalizumab(in house)投与によって体温が上昇傾向を示しました。Omalizumab(in house)は、B-hIgE/hFCER1Aマウス(H/H、H/H)におけるASAモデルによる体温低下を抑制する効果があることが確認されました。
| T1/2 (day) | CL (mL/day) | |||
| B-hFcRn | C57BL/6 | B-hFcRn | C57BL/6 | |
| Ab1 | 8.9 | 10.4 | 0.312 | 0.264 |
| Ab1-YTE | 12.7 | 4.1 | 0.072 | 0.36 |
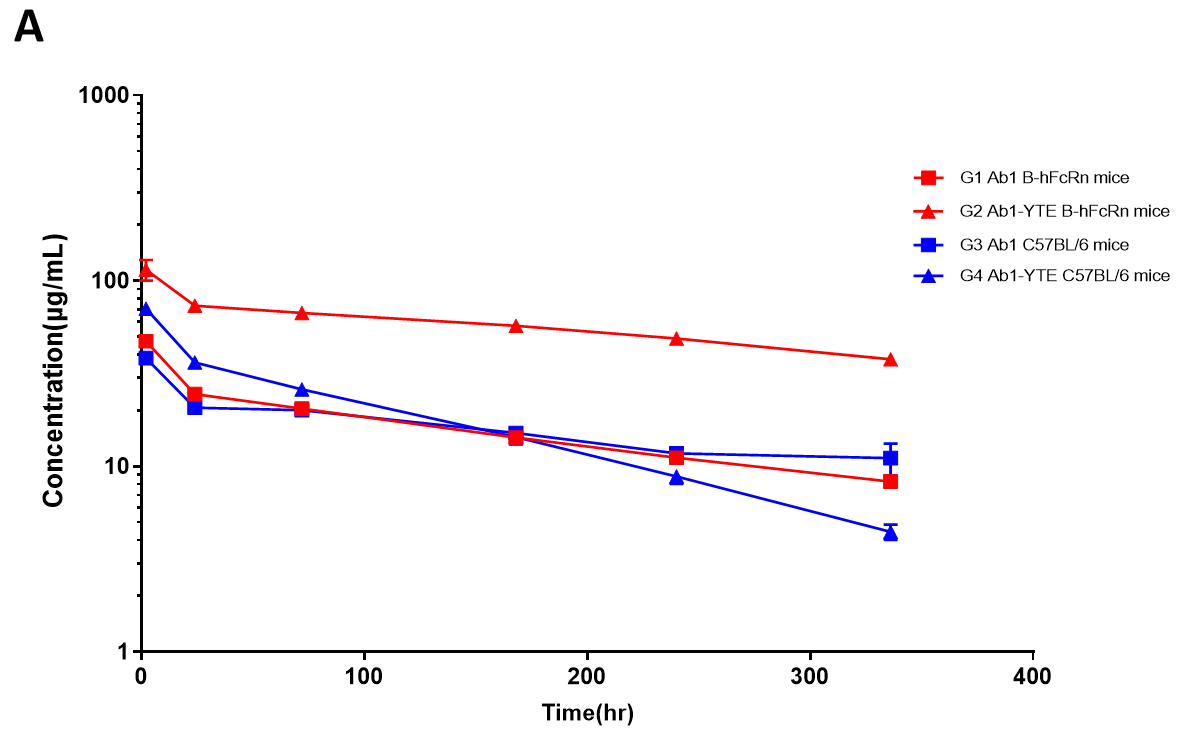
Ab1とAb1-YTEの血清薬物動態曲線が示されています。YTEによる抗体半減期の延長効果は、B-hFcRnマウスでのみ観察され、野生型マウスでは確認されませんでした。
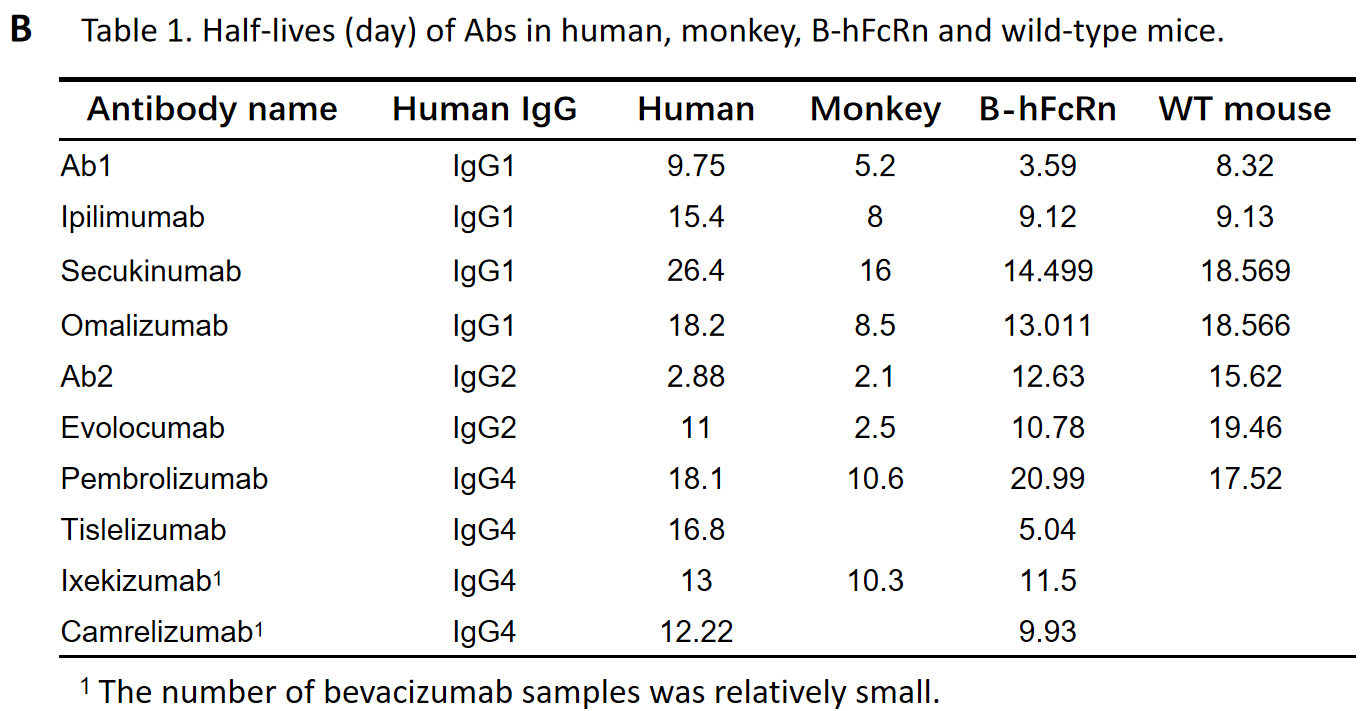
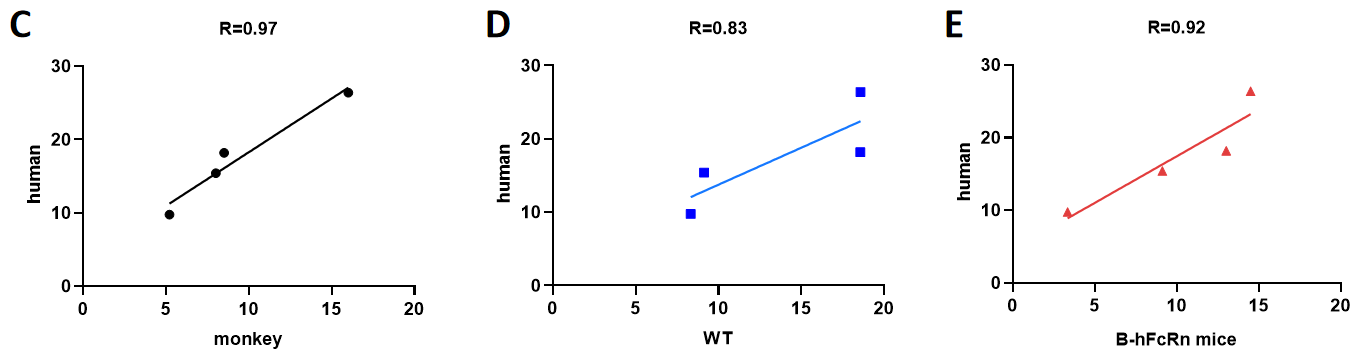
ヒトおよびサル(C)、野生型マウス(WT)(D)、B-hFcRnマウス(E)における半減期の相関関係(ヒトIgG1モノクローナル抗体のみ)。
| Product Name | Product No. | Background | Action |
| B-hC1Q mice | 111990 | C57BL/6 | |
| B-NDG FcγR KO mice | 112839 | B-NDG | |
| B-NDG hIL15, FcγR KO mice | 112653 | B-NDG | |
| huHSC-B-NDG hIL15, FcγR KO mice | 114031 | B-NDG | |
| MORE >> | |||