このページで
| Model type | Model names | Modeling reagent | Core Index | Optional tests | Model tested |
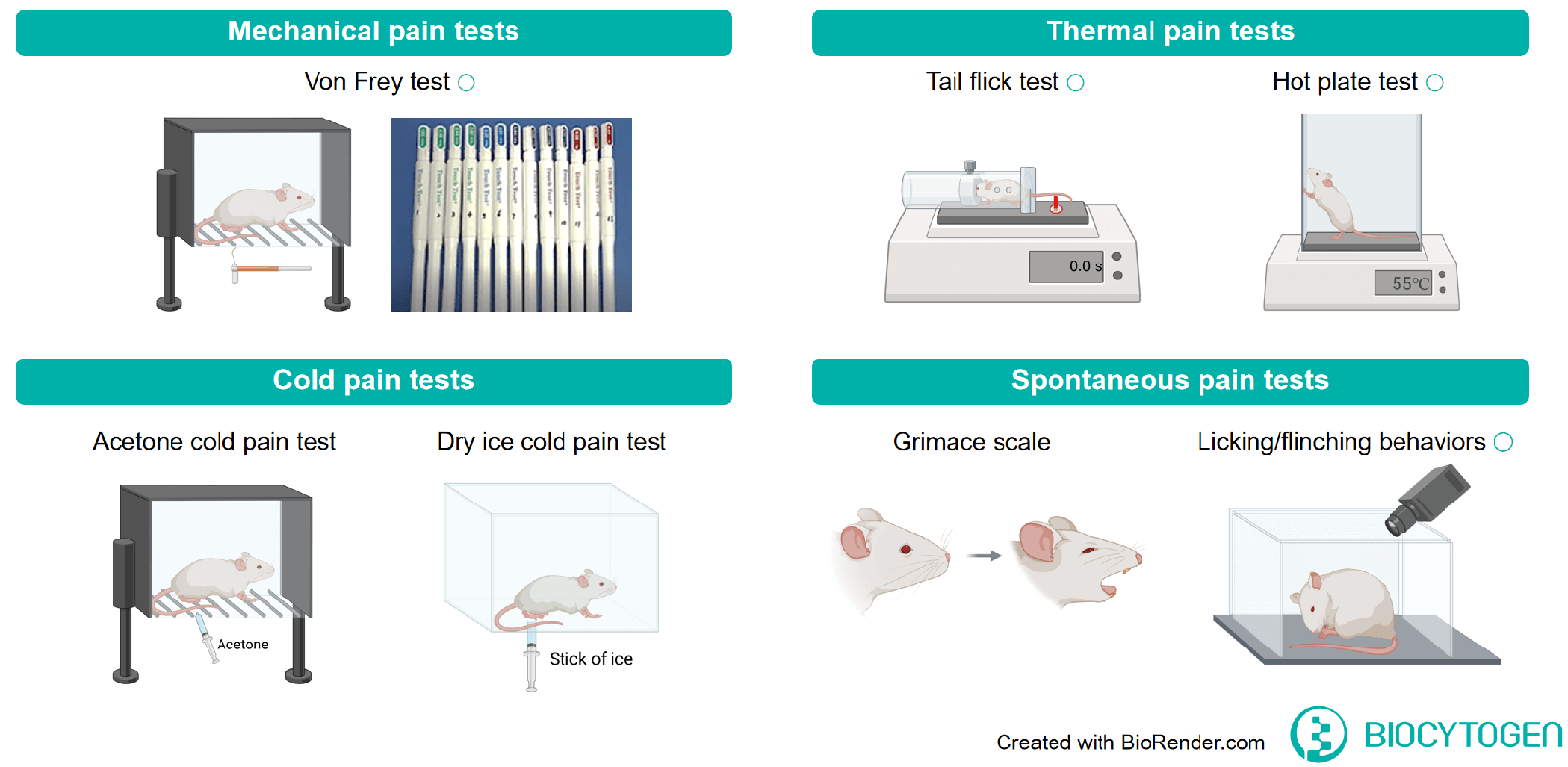
| Acute pain | Tail-flick test | - | Tail flick latency | - | C57BL/6J |
| Hot-plate test | - | Reaction latency | - | C57BL/6J | |
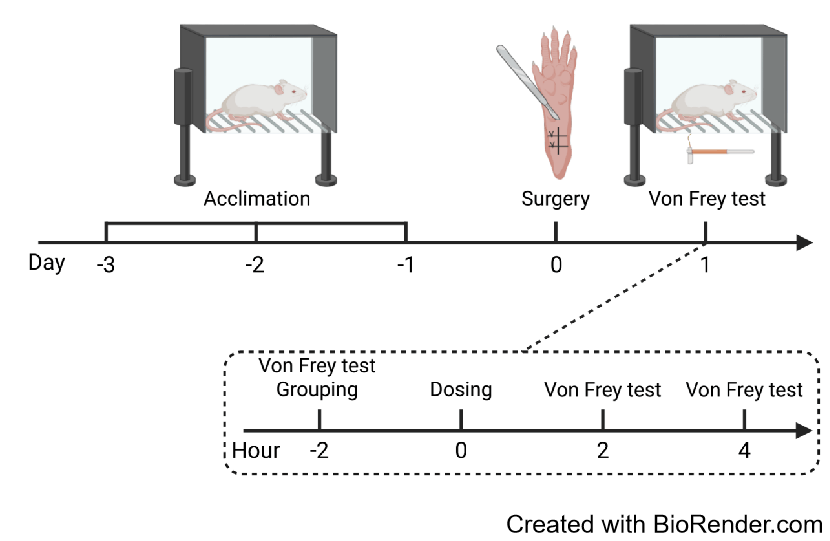
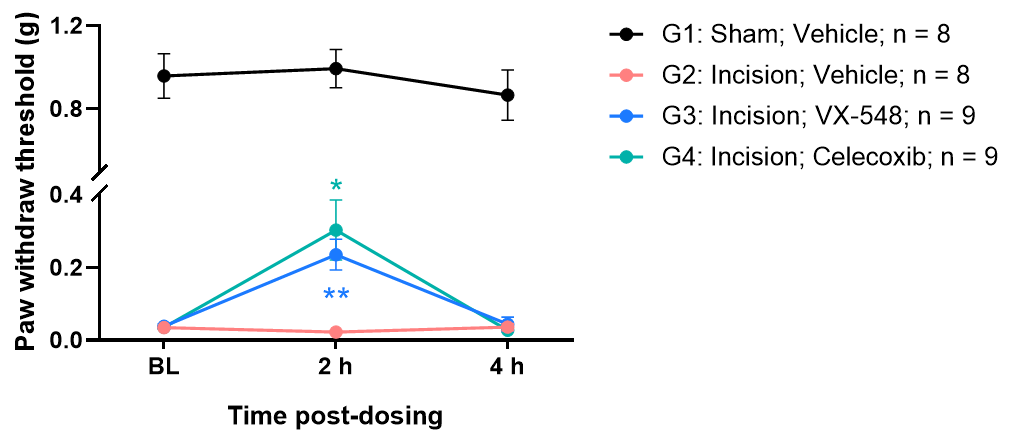
| Postoperative pain | - | Mechanical threshold | Thermal sensitivity | C57BL/6J | |
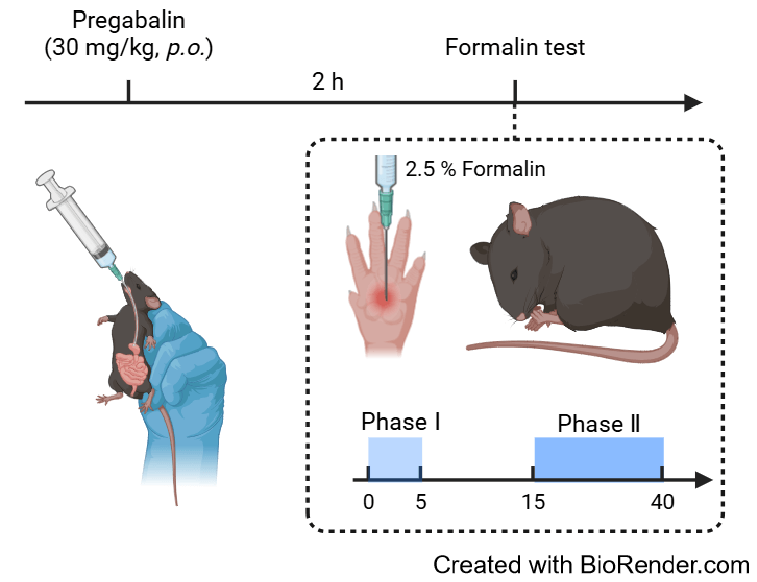
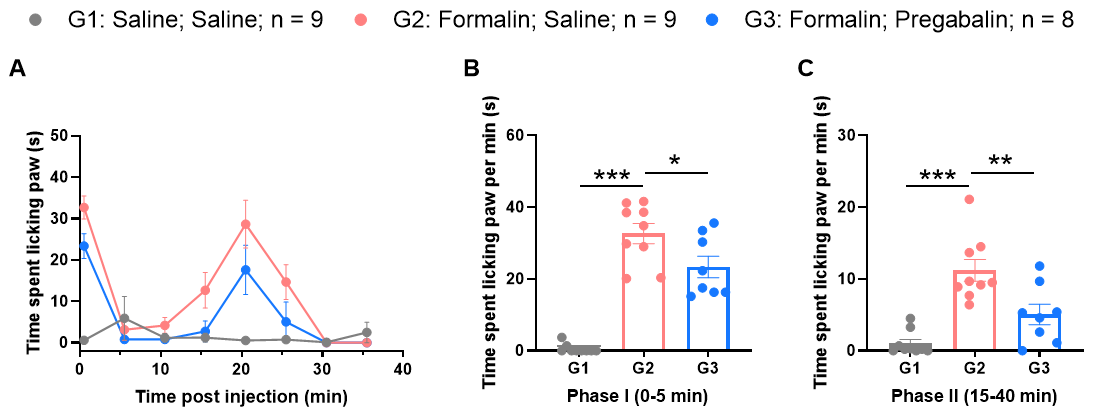
| Inflammatory pain | Formalin pain | Formalin solution | Time spent licking paw (mice) Number of flinches (rat) |
- | C57BL/6J |
| Acetic acid induced visceral pain | Acetic acid | Number of writhing episodes | - | Under development | |
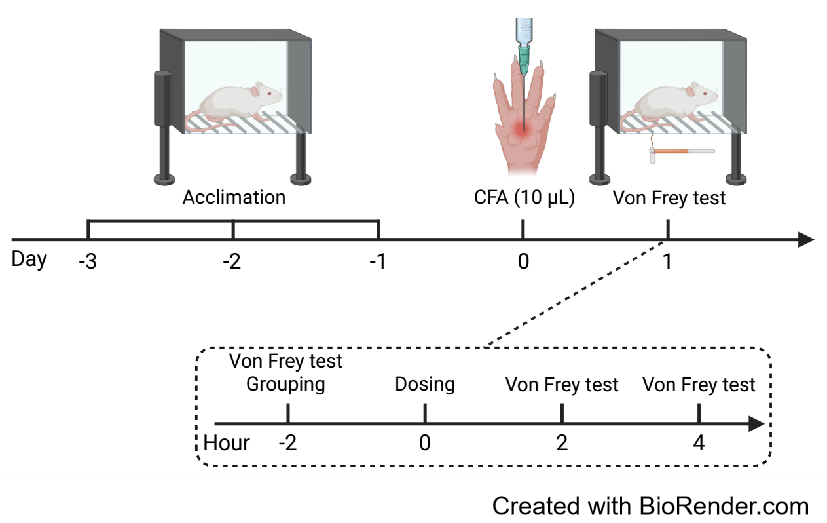
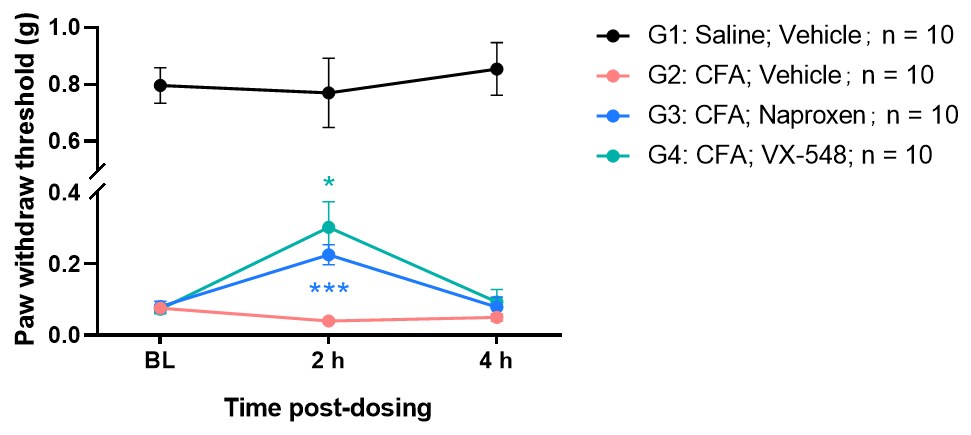
| CFA induced inflammatory pain | Complete Freund's Adjuvant | Mechanical threshold | Thermal sensitivity Cold sensitivity |
C57BL/6J; ICR | |
| Neuropathic pain | Spared nerve injury | - | Mechanical threshold | Thermal sensitivity Cold sensitivity |
Under development |
| Chronic constriction injury | - | Mechanical threshold | Thermal sensitivity Cold sensitivity |
Under development | |
| Spinal nerve ligation | - | Mechanical threshold | Thermal sensitivity Cold sensitivity |
Under development | |
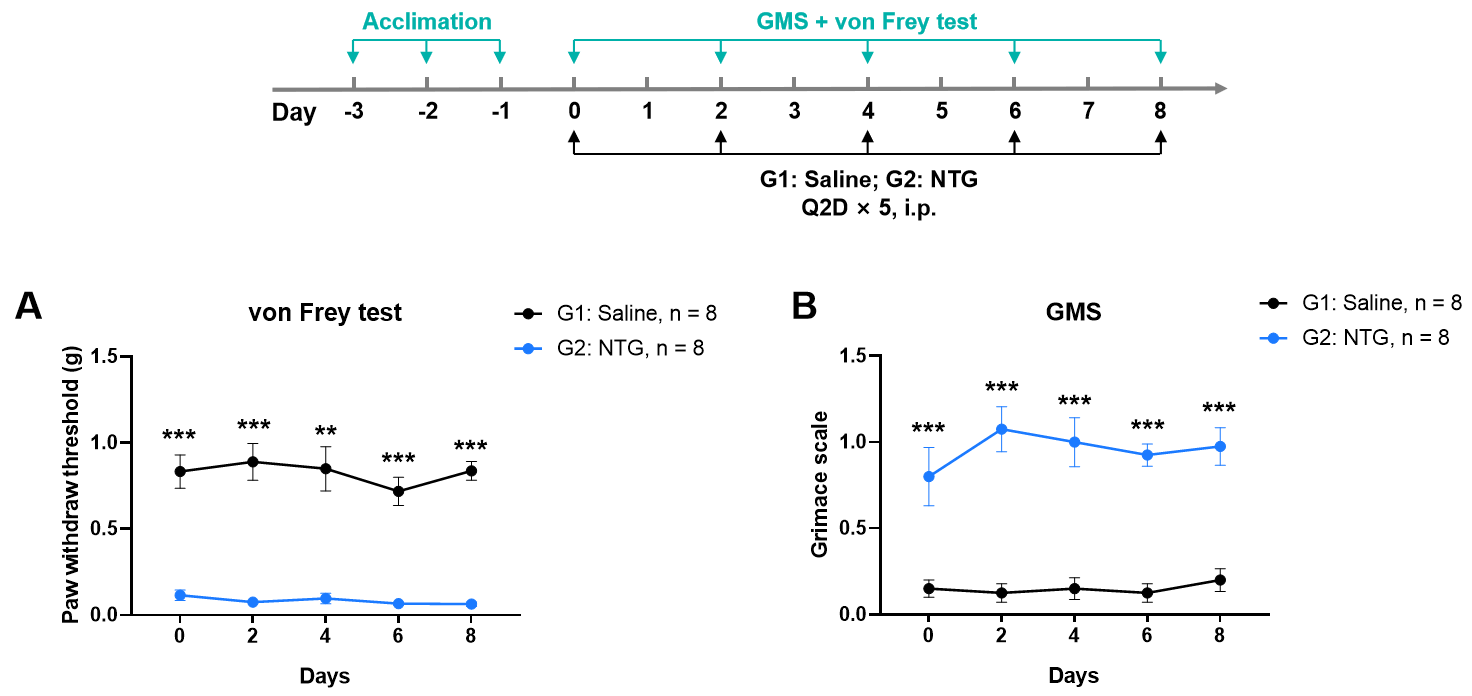
| Migraine | NTG-induced migraine | Nitroglycerin | Mechanical threshold | Grimace scale | C57BL/6J |