このページで
同系モデルは、腫瘍を遺伝的背景が同一の免疫担当マウスに移植して作製されるモデルで、研究者が完全に機能する免疫システム内で腫瘍と免疫の相互作用を研究し、免疫治療の効果を評価することを可能にします。これらの同系マウスモデルは、免疫応答、薬剤効果、および併用治療戦略の評価のために、生理学的関連性の高い生体内プラットフォームを提供し、自然な免疫-腫瘍ダイナミクスを保持し、臨床前免疫腫瘍学研究を支援します。
マウスの相同タンパク質をヒトタンパク質に置き換えることで、遺伝子ヒト化マウスモデルは交差反応の制約を克服し、ヒトまたはヒト化抗体医薬の薬効試験における評価を可能にします。これにより、代替抗体への依存を低減し、臨床前研究の臨床転換関連性を高めます。免疫不全マウスを用いたヒト免疫再構成モデルに比べ、これらの標的ヒト化マウスモデルはより高いコスト効率と、より一貫した実験結果を提供します。
イノベーティブな医薬品開発に対する増大する需要に応えるため、バイオサイトジェン(Biocytogen)は単一、二重または多重の免疫関連経路を標的とする、幅広いラインナップのヒト化マウスモデルを開発しています。さらに、潜在的な薬剤作用メカニズムに基づき、対応するヒト化腫瘍細胞株を確立しており、薬効評価のためにより総合的で臨床転換関連性の高い生体内モデルを提供しています。
ヒト化 CD40 マウスのケーススタディ
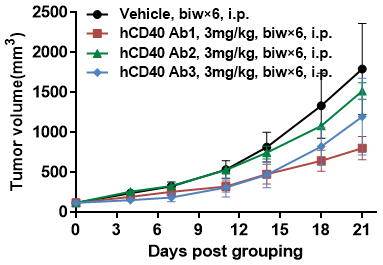
B-hCD40 マウスにおける抗ヒト CD40 抗体の抗腫瘍活性
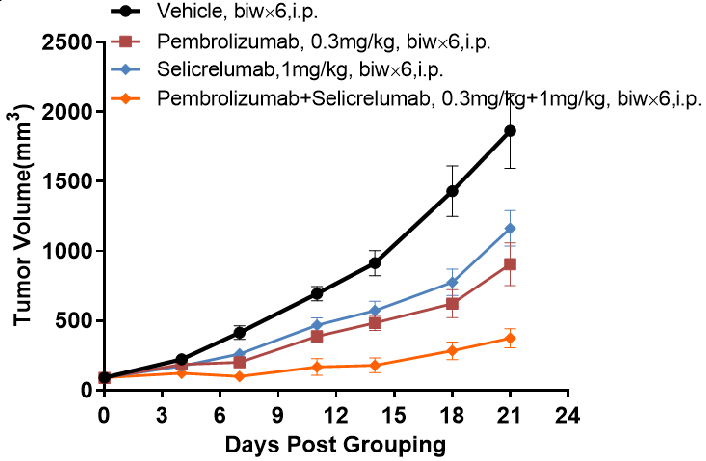
B-hPD-1/hPD-L1/hCD40マウスにおけるPembrolizumabとSelicrelumabの抗腫瘍活性
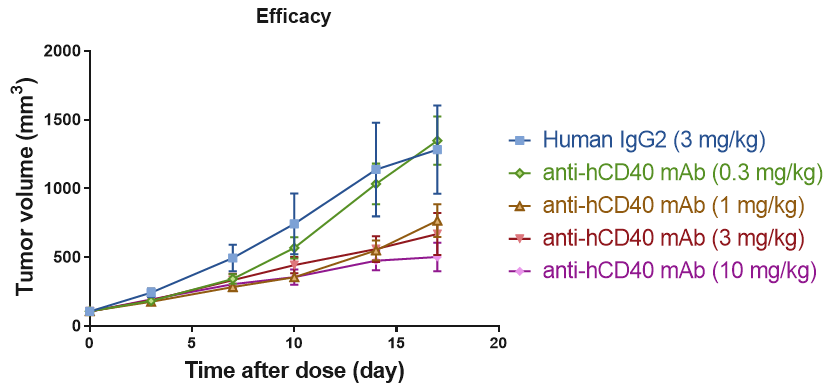
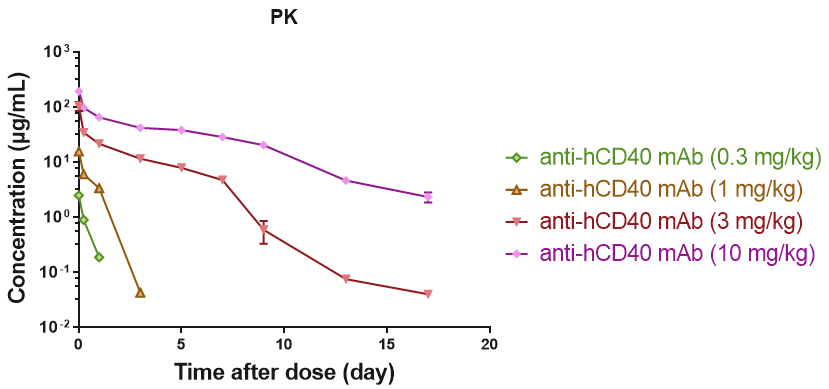
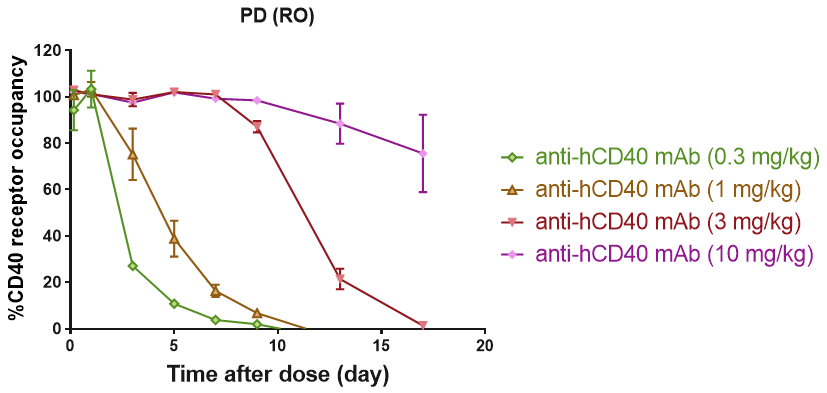
B細胞CD40受容体のRO