このページで
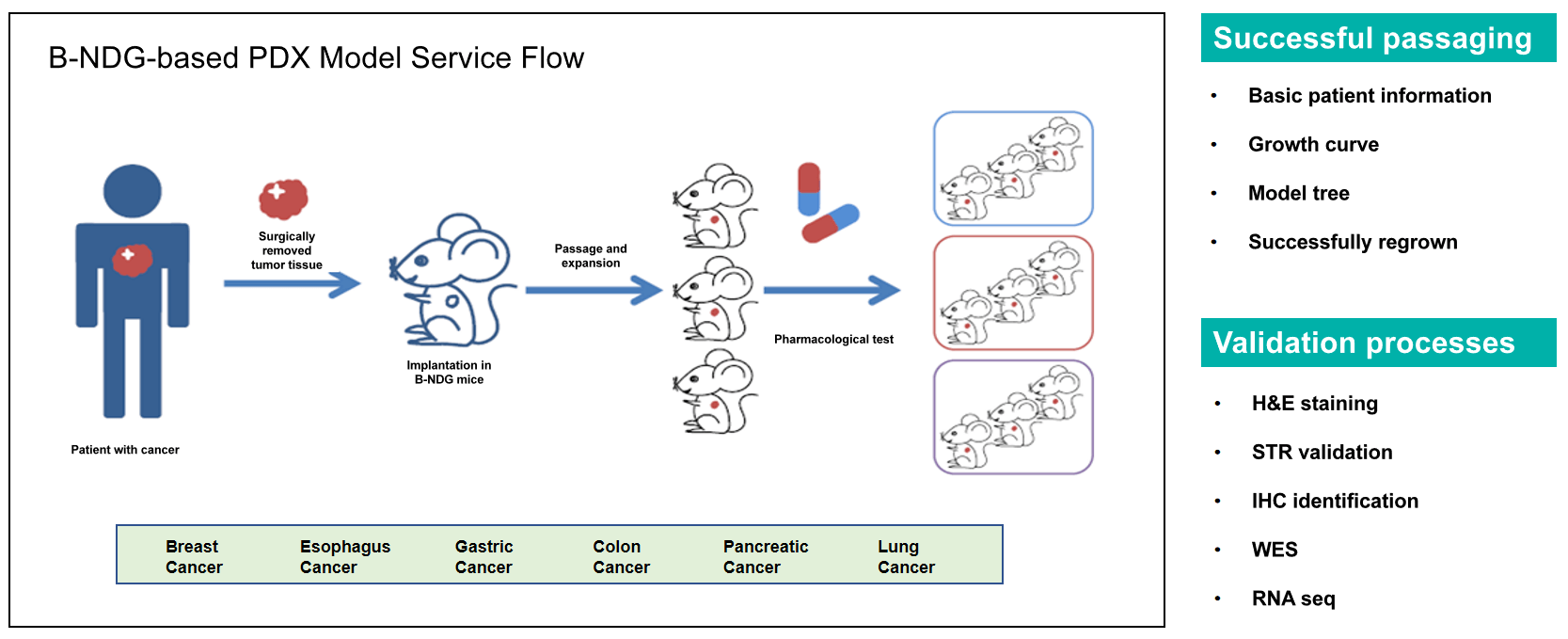
患者由来異種移植(PDX)モデルは、患者の腫瘍サンプルを免疫不全マウスに移植して作製されるモデルで、ヒトがんの特徴を効果的に再現します。バイオサイトジェン(Biocytogen)は、最適化された PDX 移植プロセスと先進技術を活用し、生体内腫瘍学研究のために高い信頼性を持つ異種移植マウスモデルを提供しています。これらの PDX モデルは、新規抗がん薬の臨床前評価、併用治療法の有効性検証、薬剤感受性患者集団の特定、および薬剤耐性メカニズムの研究のための強力なプラットフォームとして機能します。
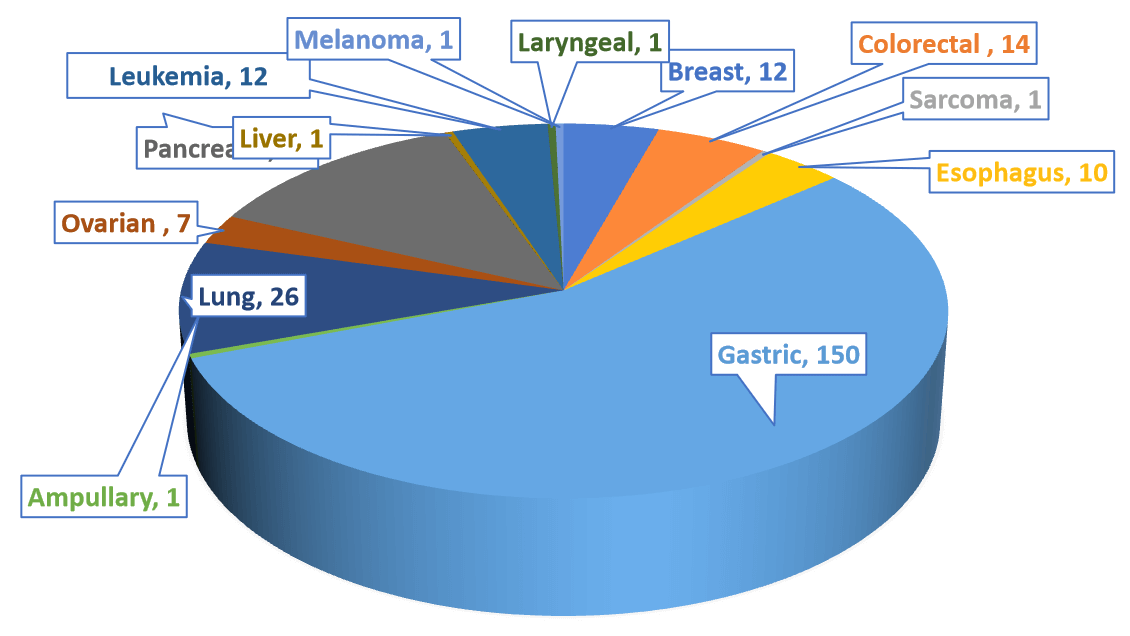
Biocytogenで270個のPDXモデルが成功裏に確立され、そのうち13種類の癌が含まれている。
| Experienced in ADC evaluation | Immune reconstitution | High quality PDX from vendors | Gene expression database | Live PDX animal |
|
|
|
|
|
| Types of cancer | Model quantity | TMA quantity |
| Breast | 12 | 1 |
| Colorectal | 13 | 2 |
| Esophagus | 10 | 1 |
| Gastric | 144 | 13 |
| Lung | 22 | 3 |
| Pancreatic | 34 | 4 |
| Ampullary | 1 | 1 |
| Targets tested by IHC | |||||
| HER2 | CDCP1 | 5T4 | EPHA2 | CLDN18.2 | LYPD3 |
| MSLN | HER3 | PTK7 | ADAM9 | TIM1 | PSCA |
| MUC16 | EGFR | ITGB6 | B7-H3 | SLC34A2 | KREMEN2 |
| TPBG | MET | MUC1 | B7-H4 | CD71 | CD228 |
| FOLR1 | EPCAM | TROP2 | GPC1 | CDH3 | MUC18 |
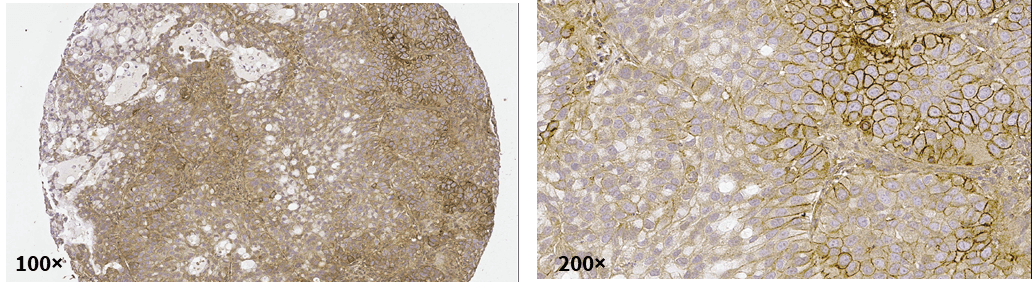
| Model ID | BP0508 |
| Cancer type | Lung cancer |
| Rating scale | 3+ |
| Generation | R5P4 |
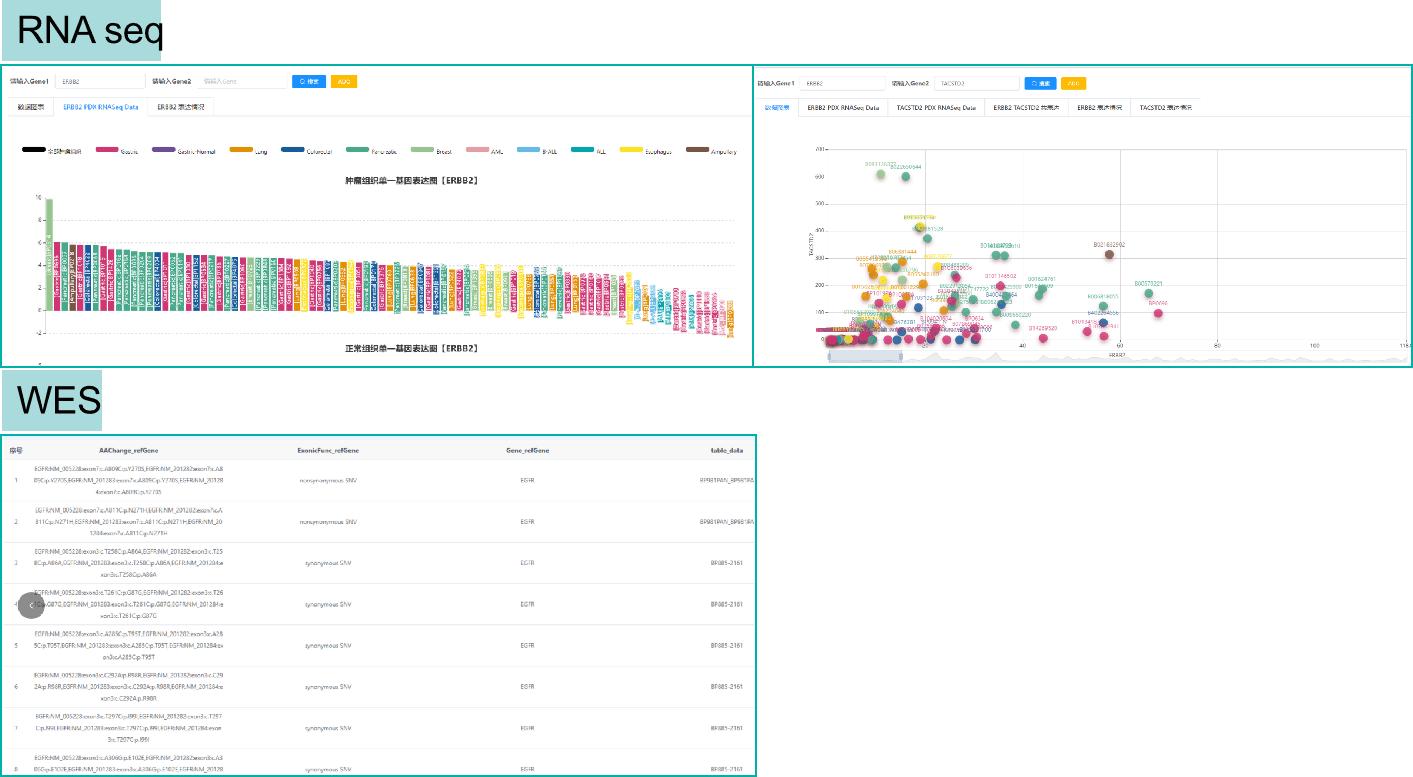
PDX Seqデータベース
| Model ID | Subtype analysis | Gender/Age | Sample Location | Type of deregulations | TNM | CLDN18.2/EGFR | Sequencing |
| BP0062 | Ductal Adenocarcinoma | F/61 | Pancreaticoduodenal | Moderately differentiated | IV | positive | WES |
| HLA-A | HLA-B | HLA-C | HLA-DPA1 | HLA-DPB1 | HLA-DQA1 | HLA-DQB1 | HLA-DRA | HLA-DRB1 | HLA-DRB3 | HLA-DRB4 | |
| BP0062-P0 | 02:242 | 40:06 | 08:01 | 02:02 | 05:01 | 01:02 | 06:02 | 01:01 | 15:01 | 01:01 | 01:01 |
| 01:215 | 37:01 | 06:138 | 01:03 | 22:01 | 04:01 | 03:01 | 07:01 | 02:02 |
STR確認
| Genetic Site | BP0062-P1 | BP0062-P5 | ||
| Amelogenin | X | X | X | X |
| CSF1PO | 10 | 12 | 10 | 12 |
| D13S317 | 10 | 10 | ||
| D16S539 | 9 | 12 | 9 | 12 |
| D5S818 | 11 | 11 | ||
| D7S820 | 9 | 12 | 9 | 12 |
| TH01 | 9 | 9 | ||
| TPOX | 8 | 11 | 8 | 11 |
| vWA | 12 | 17 | 12 | 17 |
| D21S11 | 30 | 32.2 | 30 | 32.2 |
ANSIによって確立された国際基準に従い、細胞株の一致度が≥80%であれば、それらは関連があると見なされます。結果は、これらのサンプルが100%の一致度を持ち、同一患者からのものであることを示しました。
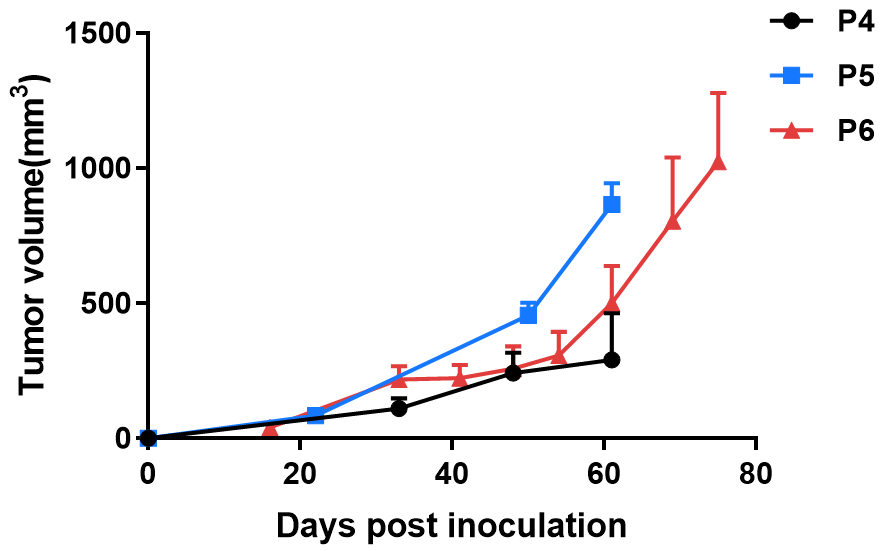
BP0062はB-NDGマウスに皮下注射されました。腫瘍体積は式V=0.5a X b2を使用して計算され、aとbは腫瘍の長径と短径です。データは平均±SEMで示されています。
結果:膵臓癌PDXモデルBP0062は、B-NDGマウスで成功裏に確立されました。腫瘍体積を効果的に追跡できます。
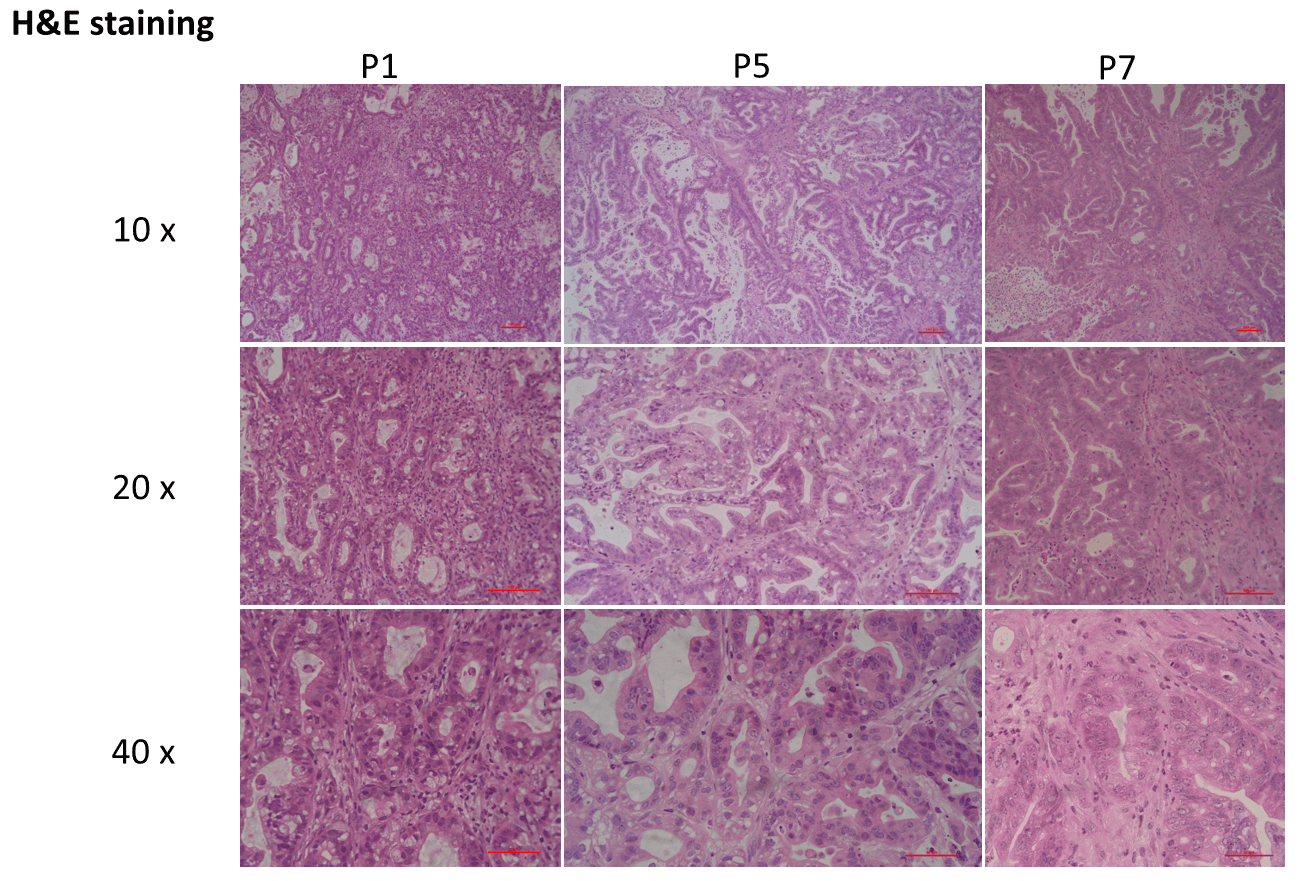
患者由来異種移植モデルは、元の患者サンプルの構造を再現し、異なる世代において同様の異質性を保持することがわかりました。
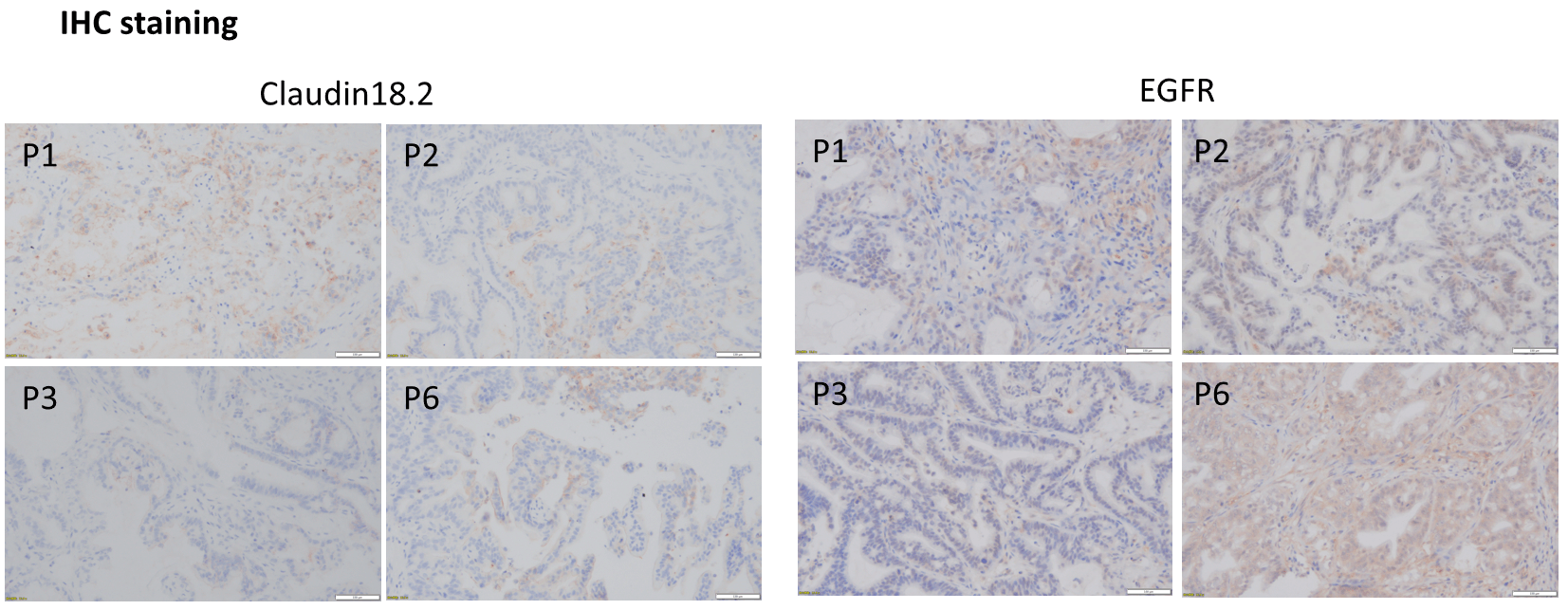
CLDN18.2とEGFRのIHC評価では、異なる世代の個々の腫瘍において異質性は観察されませんでした。
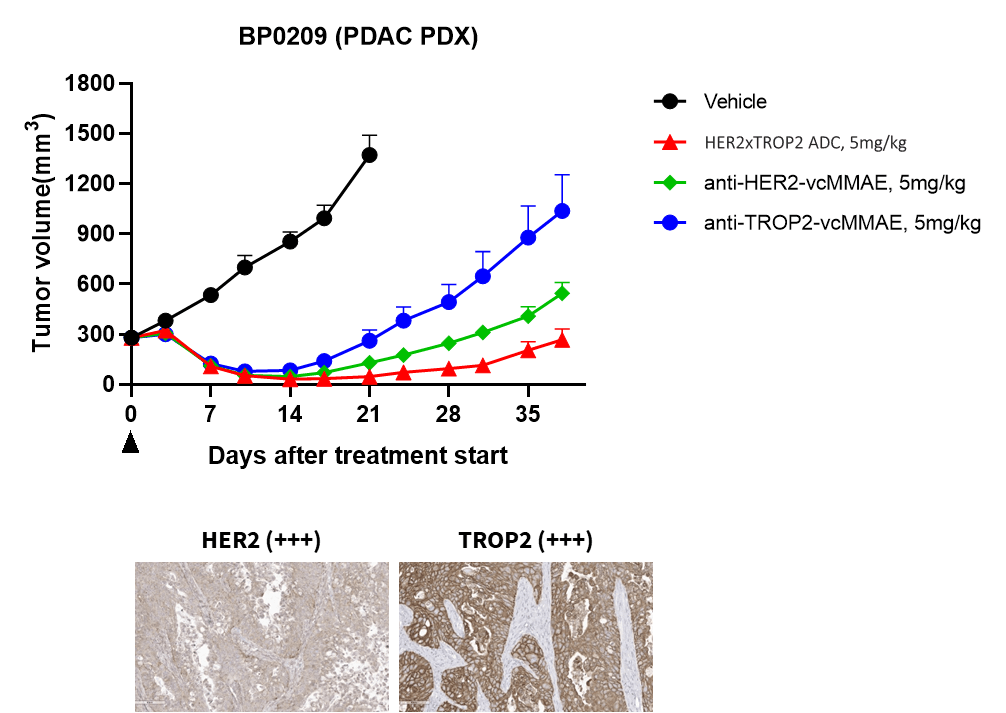
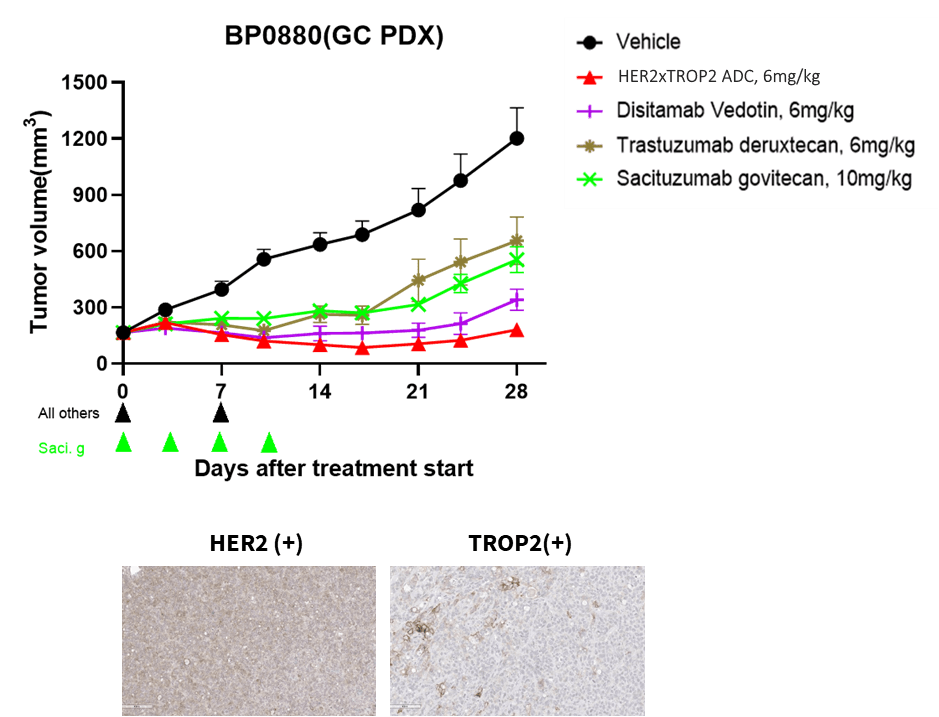
Her2 x Trop2 ADCは、Her2/Trop2高発現および低発現のPDXモデルの両方で著しい腫瘍成長抑制を示しました。
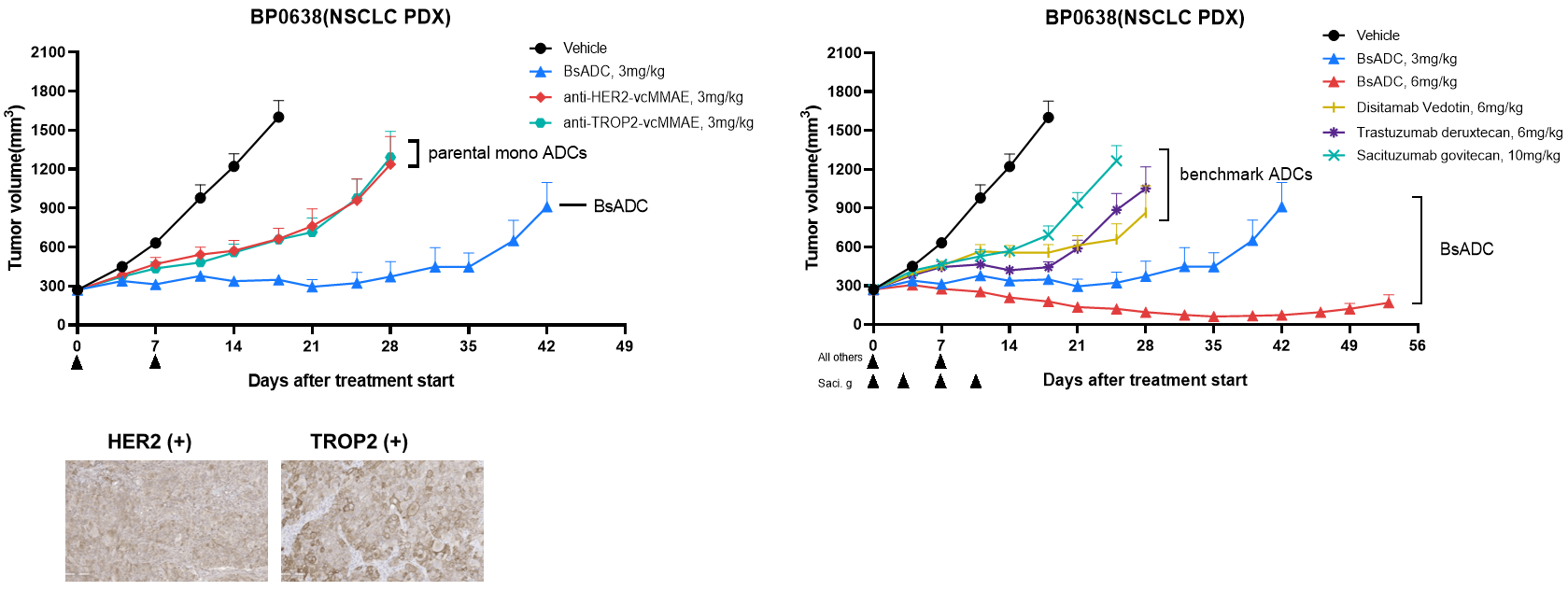
HER2低発現PDXモデルにおいて強力で持続的な抗腫瘍活性を示しました。BsADCは、親株の単一ターゲットADCおよび基準となるADCと比較して、HER2低発現の非小細胞肺癌(NSCLC)PDXモデルにおいて強力で持続的な抗腫瘍活性を示し、BsADCが腫瘍異質性によって引き起こされる単一ターゲットADCの耐性を克服する強力な治療の可能性を持っていることを示しています。
| Model ID | Subtype | Information about patient | Growth curve | Pn≥3 | STR analysis | HLA | WES | RNA-Seq | In vivo study |
| BP2010 | AML-M5 | √ | √ | √ | √ | √ | √ | √ | √ |
| BP2035 | AML-M2 | √ | √ | √ | √ | √ | |||
| BP2053 | B-ALL | √ | √ | √ | √ | √ | √ | √ | |
| BP2055 | B-ALL | √ | √ | √ | √ | √ | √ | √ | √ |
| BP2075 | B-ALL | √ | √ | √ | √ | √ | |||
| BP2084 | T-ALL | √ | √ | √ | √ | √ | √ | √ | √ |
| BP2088 | B-ALL | √ | √ | √ | √ | √ | √ | ||
| BP2094 | B-ALL | √ | √ | √ | √ | √ | √ | √ | |
| BP2097 | B-ALL | √ | √ | √ | √ | √ | √ | √ | |
| BP2101 | B-ALL | √ | √ | √ | √ | √ | √ | √ | √ |
| BP2103 | AML-M4 | √ | √ | √ | √ | √ | √ | √ | √ |
| BP2117 | AML FLT3+ | √ | √ | √ | √ | √ |
| Model ID | Subtype analysis | Gender/Age | Source type | Immunophenotyping | Fusion gene | SNV |
| BP2010 | Relapse refractory AML-M5 | F/60 | Peripheral Blood | Express: HLA-DR (85.6%), CD34 (85.8%), CD13 (72.3%), CD33 (87.5%), CD117 (88.4%), CD64 (56%), CD38 (99.5%); Not express: CD10, CD19, CD20, CD22, CD2, CD3, CD4, CD5, CD7, CD8, CD14, CD15, CD11b, CD56, MPO, cCD79a,cCD3 |
MLL-AF6 positive | NRAS Q61R Mutation positive |
| HLA-A | HLA-B | HLA-C | HLA-DPA1 | HLA-DPB1 | HLA-DQA1 | HLA-DQB1 | HLA-DRA | HLA-DRB1 | HLA-DRB4 | |
| BP2010 | 29: 01 | 07: 05 | 15: 05 | 01: 03 | 03: 01 | 01: 02 | 06: 02 | 01: 01 | 15: 01 | 01: 01 |
| 26: 01 | 48: 05 | 02: 140 | 03: 01 | 02: 02 | 03: 01 | 03: 01 | 04: 07 |
STR確認
| Genetic Site | BP2010-PA | BP2010-P9 | ||
| Amelogenin | X | X | X | X |
| CSF1PO | 12 | 12 | 12 | 12 |
| D13S317 | 8 | 11 | 8 | 11 |
| D16S539 | 10 | 11 | 10 | 11 |
| D5S818 | 9 | 11 | 9 | 11 |
| D7S820 | 10 | 13 | 10 | 13 |
| TH01 | 9 | 9 | 9 | 9 |
| TPOX | 8 | 11 | 8 | 11 |
| vWA | 14.2 | 15.2 | 15 | 16 |
| D21S11 | 29 | 29 | 29 | 29 |
ANSIによって確立された国際基準に従い、細胞株の一致度が≥80%であれば、それらは関連していると見なされます。結果は、これらのサンプルが100%一致しており、同一の個体からのものであることを示しています。
細胞表現型の確認
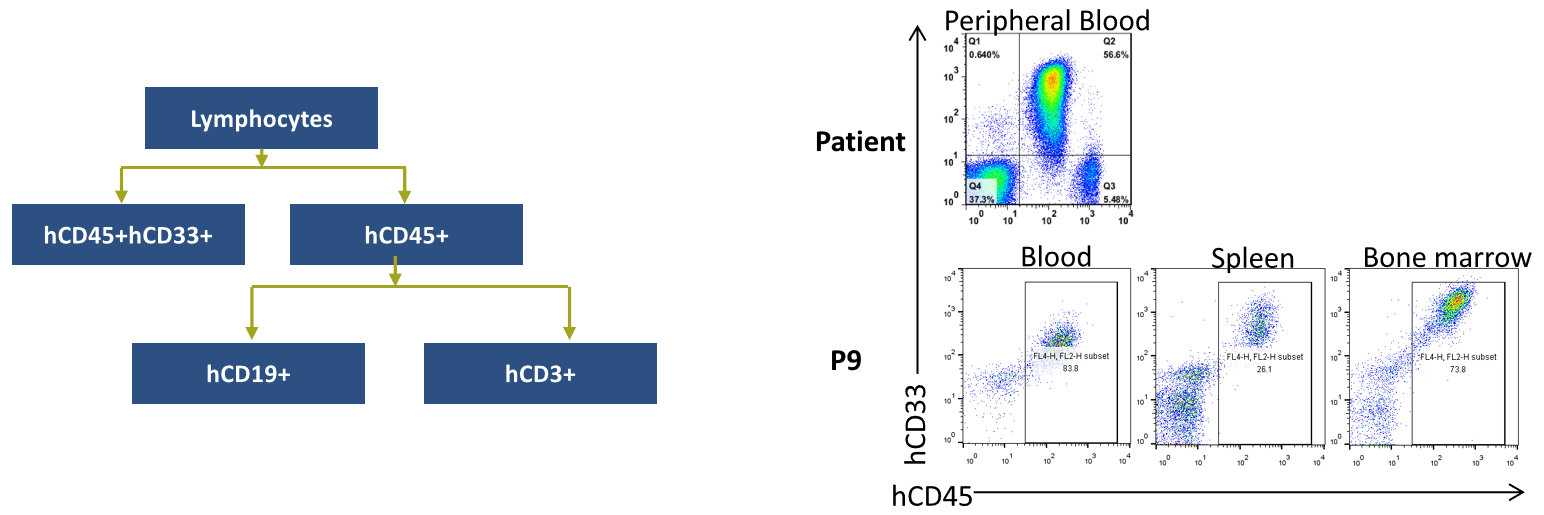
対象個体由来の異種移植モデルは、異なる世代において免疫表現型を再現できることが確認されました。
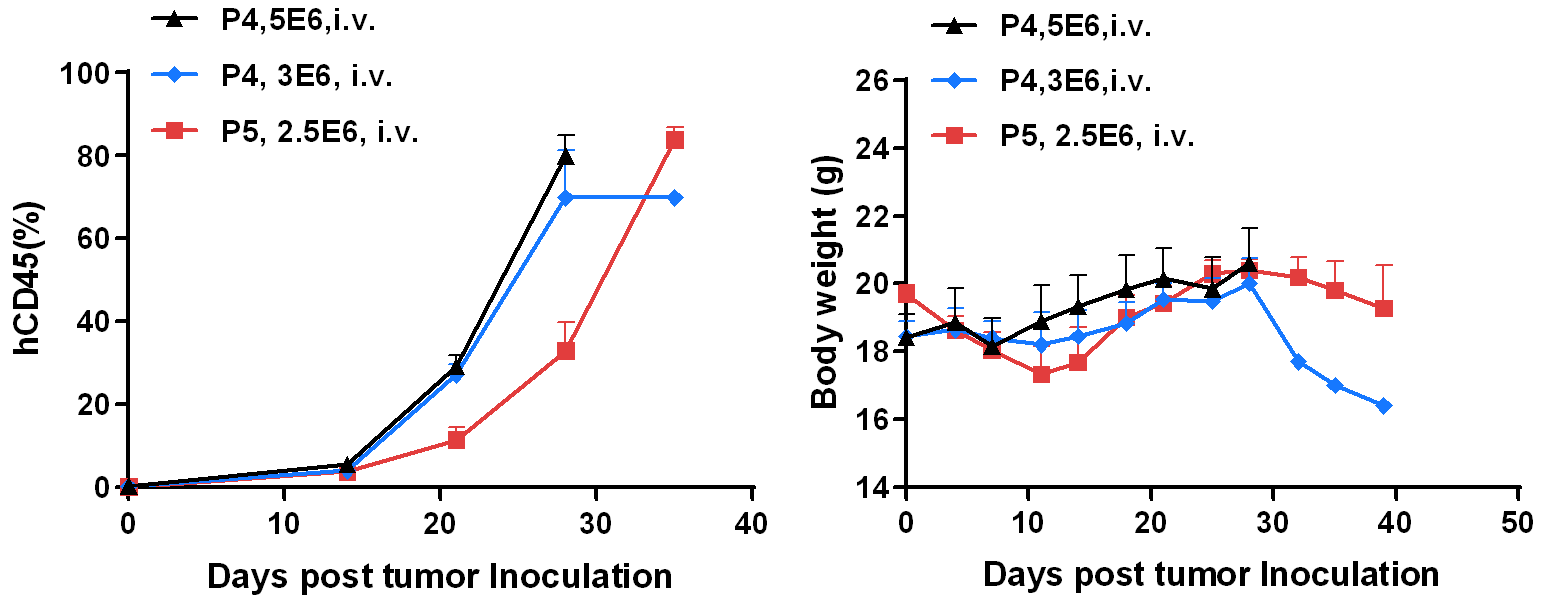
血液サンプル中のhCD45濃度は、フローサイトメトリーで分析しました。体重は週2回測定しました。データは平均値±標準誤差(SEM)で表示されます。
結果: BP2010の白血病PDXモデルは、B-NDGマウスで成功裏に確立され、hCD45の割合を効果的に追跡できます。
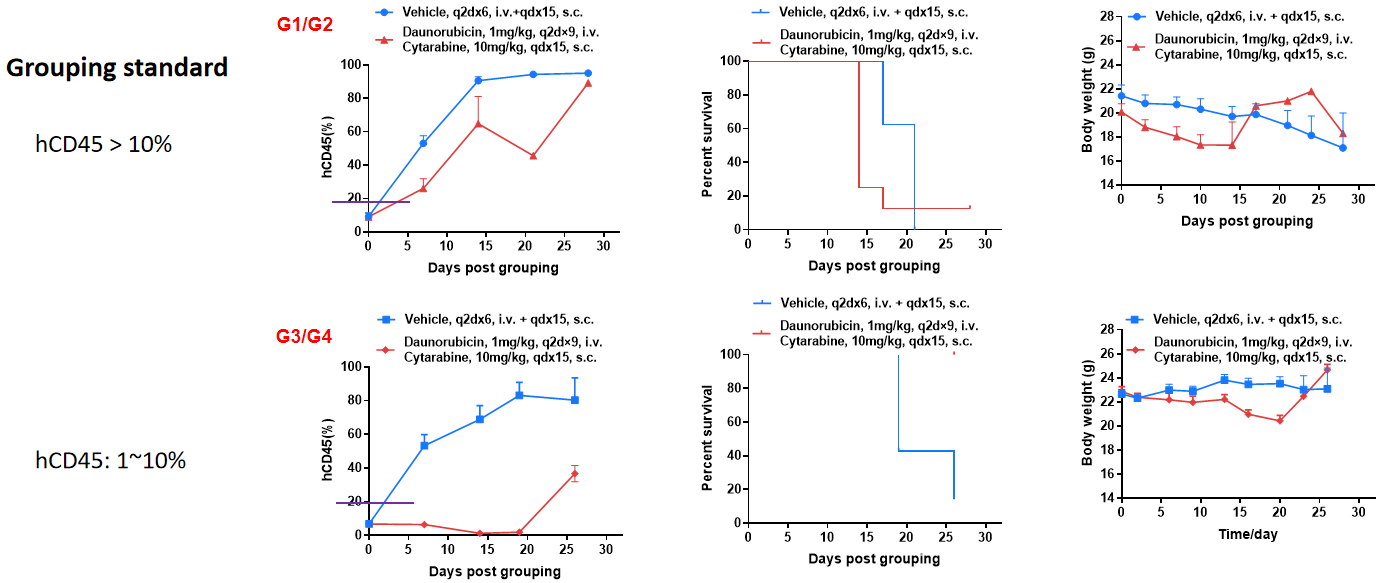
hCD45 > 10%の場合、治療群に顕著な効果は見られませんでした;10% > hCD45 > 1%の場合、治療群において腫瘍抑制効果が顕著でした。
結論:投与中のモデリングの程度は、低分子薬の有効性に大きな影響を与えることがわかりました。
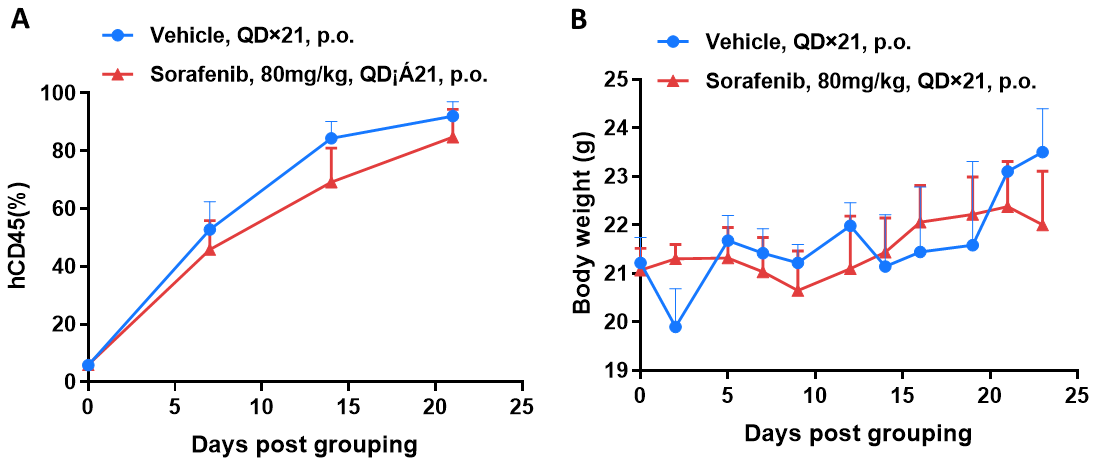
B-NDGマウスにおけるFLT3をターゲットにした薬物の抗腫瘍活性 (A) 分子ターゲット型低分子抗癌薬は、B-NDGマウスにおけるBP2010の腫瘍成長をわずかに阻害しました。BP2010のPDXモデルは、B-NDGマウスの尾静脈に投与されました(雌、n=6)。PBのhCD45陽性細胞が約10%に達した時点でマウスをグループ分けし、図に示す薬剤および投与スケジュールで投与しました。(B)投与中の体重変化。データは平均±SEMで表示されます。
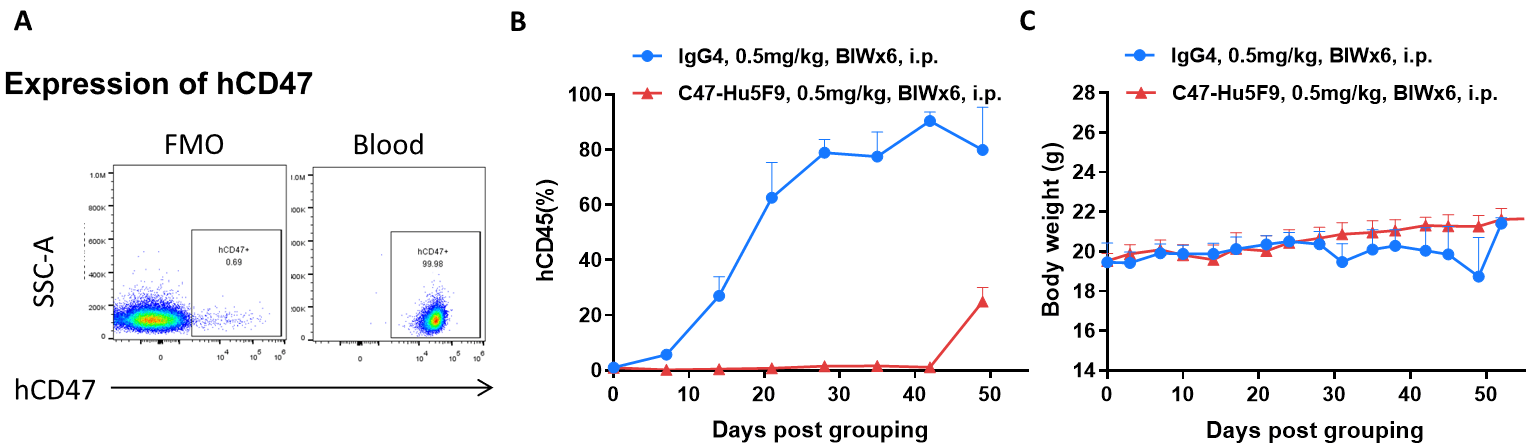
抗体のB-NDGマウスにおける抗腫瘍活性 (A) BP2010腫瘍細胞表面で人CD47が高度に発現していました。(B) 抗体CD47-Hu5F9は、B-NDGマウスにおけるBP2010の腫瘍成長を阻害することができました。BP2010のPDXモデルは、B-NDGマウスの尾静脈に投与されました(雌、n=7)。PBのhCD45陽性細胞が約1%に達した時点でマウスをグループ分けし、図に示すスケジュールで抗体薬を投与しました。(C)投与中の体重変化。データは平均±SEMで表示されます。