このページで
代謝異常関連脂肪性肝炎(MASH)は、旧称を非アルコール性脂肪性肝炎(NASH)とし、非アルコール性脂肪性肝疾患(NAFLD)の範囲内に含まれる進行性の代謝性肝疾患です。この疾患は肝脂肪症、炎症、肝細胞障害、線維化を特徴とし、肝硬変や肝細胞がんへ進行する可能性があります。肥満症、インスリン抵抗性、2 型糖尿病が併存する場合、疾患の発症リスクと進行リスクが大幅に高まります。
臨床的には、MASH は脂肪性肝炎、肝細胞の气球様変性、肝線維化、代謝機能異常を伴います。疾患メカニズムをより深く理解し、新規治療法を評価するため、MASH/NASH マウスモデルは前臨床肝疾患研究で広く使用されています。これらのモデルには、遺伝子改変型、食餌誘発型、またはこれら 2 種類を組み合わせたタイプが含まれます。
バイオサイトジェン(Biocytogen)は、MASH(代謝異常関連脂肪性肝炎)の発症メカニズムにおける異なる病期を再現した、複数の検証済みモデルを確立しています。それには以下の種類が含まれます:
これらの MASH/NASH モデルは、メカニズム研究、薬物効果試験、前臨床研究のための信頼性の高い in vivo プラットフォームを提供し、抗脂肪症薬、抗炎症薬、抗線維化薬の治療法開発を推進します。
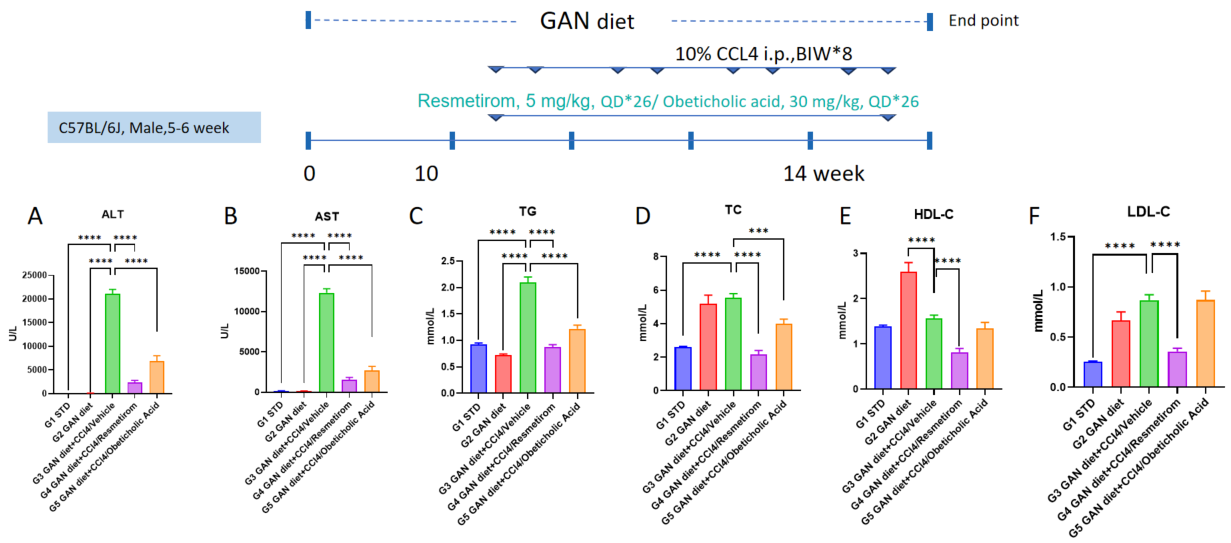
GAN 食餌+CCL4 で誘発された NASH マウスモデルにおけるMGL3196 と OCAの有効性 A-B、モデル化および治療群の ALT と AST のレベル。C-F、モデル化および治療群の TG、TC、HDL-C、LDL-C のレベル。データは平均 ± SEM として表示されています。各群 N = 9 匹のマウス。*p<0.05、**p<0.01、***p<0.001。
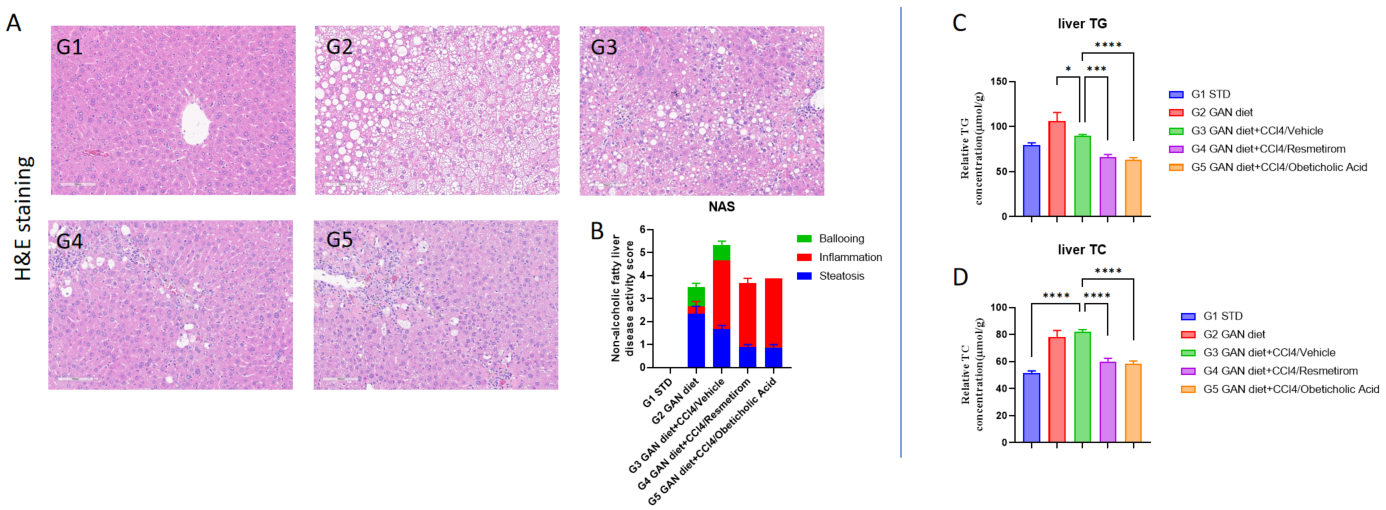
Resmetirom と OCA は 、NAS スコアを低下させました。A、H&E 染色の代表的な画像で NASH の程度を示します。B、外部の病理専門医によって評価された NAFLD 活動スコア(NAS)。C-D、治療後の肝臓内の TG と TC の含量。データは平均 ± SEM として表示されています。各群 N = 9-10 匹のマウス。*p<0.05、**p<0.01、***p<0.001。
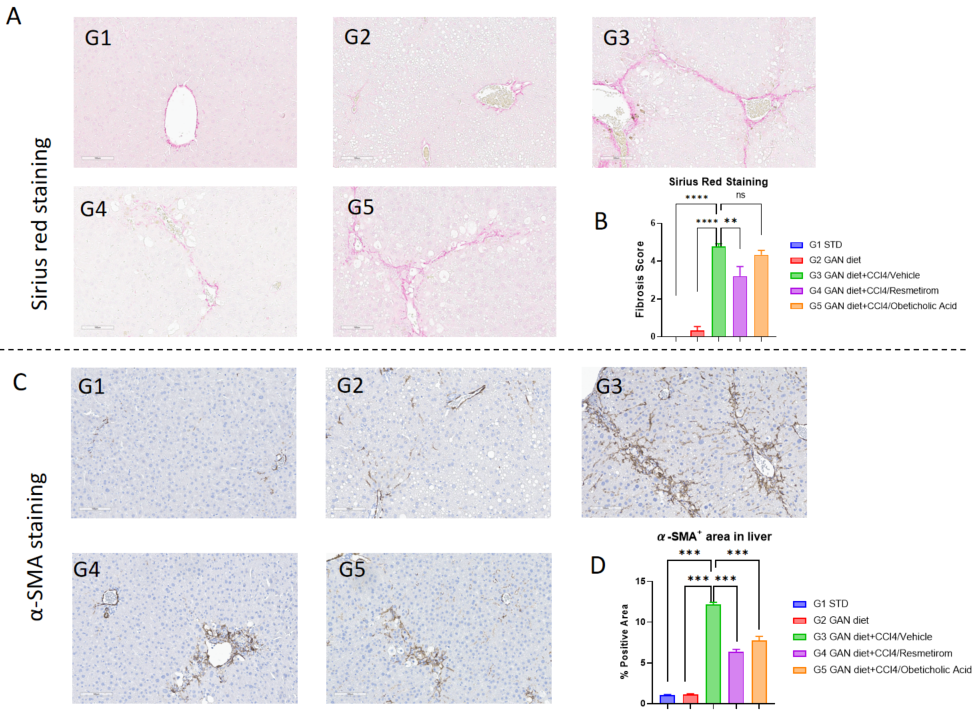
肝線維症に対するResmetirom と OCAを緩和の有効性 A、Sirius Red 染色の代表的な画像で肝線維症の程度を示します(スケールバー:200μm)。B、Sirius Red 染色に基づいて評価された肝線維症スコア。C、IHC 染色の代表的な画像で α-SMA の発現を示します(スケールバー:200μm)。D、α-SMA 発現の定量データ。データは平均 ± SEM として表示されています。各群 N = 9 匹のマウス。*p<0.05、**p<0.01、***p<0.001、****p<0.0001。

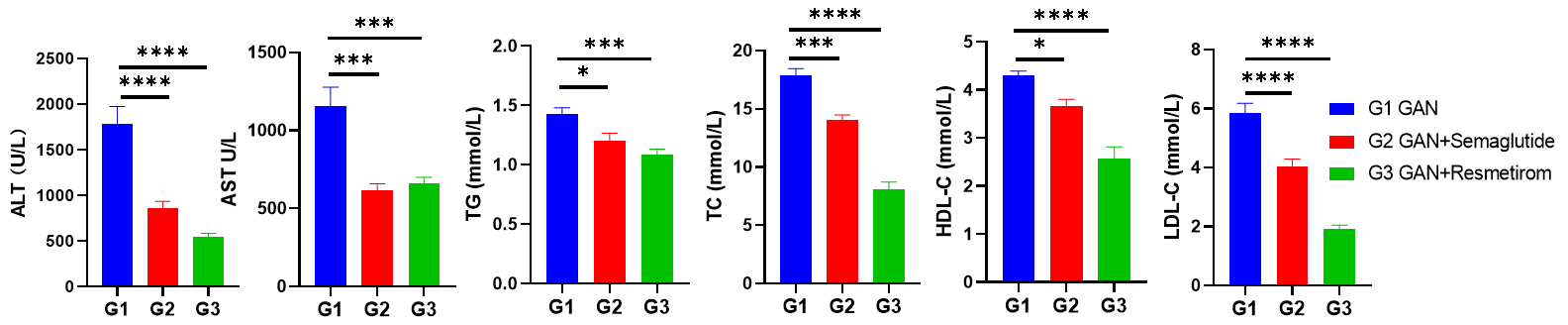
B-ob/ob マウスGubra-Amylin 食餌誘発 NASH モデルにおけるMGL3196 と Semaglutide の有効性 A-B、モデル化および治療群の ALT と AST のレベル。C-F、モデル化および治療群の TG、TC、HDL-C、LDL-C のレベル。データは平均 ± SEM として表示されています。各群 N = 9 匹のマウス。*p<0.05、**p<0.01、***p<0.001。
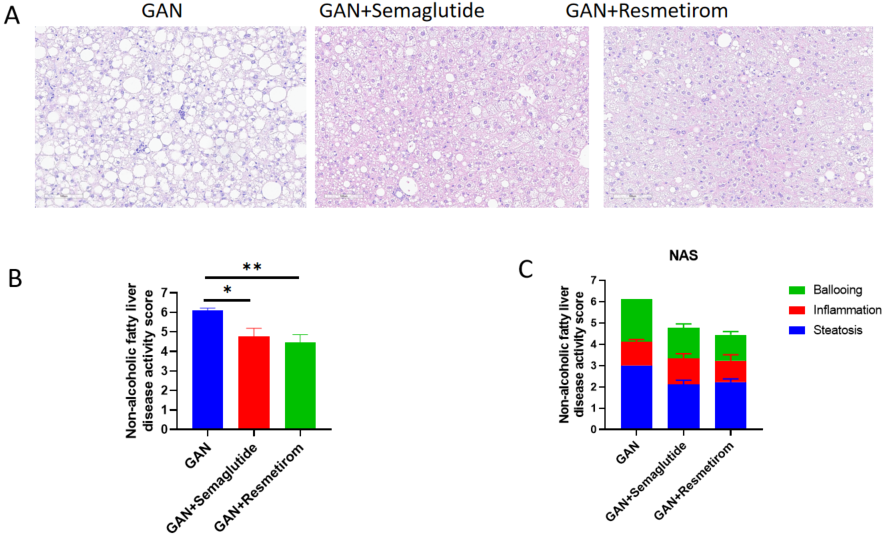
Semaglutide と Resmetirom は 、GAN 食餌誘発 B-ob/ob マウスの NAS スコアを低下させました。A、H&E 染色の代表的な画像で NASH の程度を示します。B-C、外部の病理専門医によって評価された NAFLD 活動スコア(NAS)。データは平均 ± SEM として表現されています。各群 N = 9 匹のマウス。*p<0.05、**p<0.01。
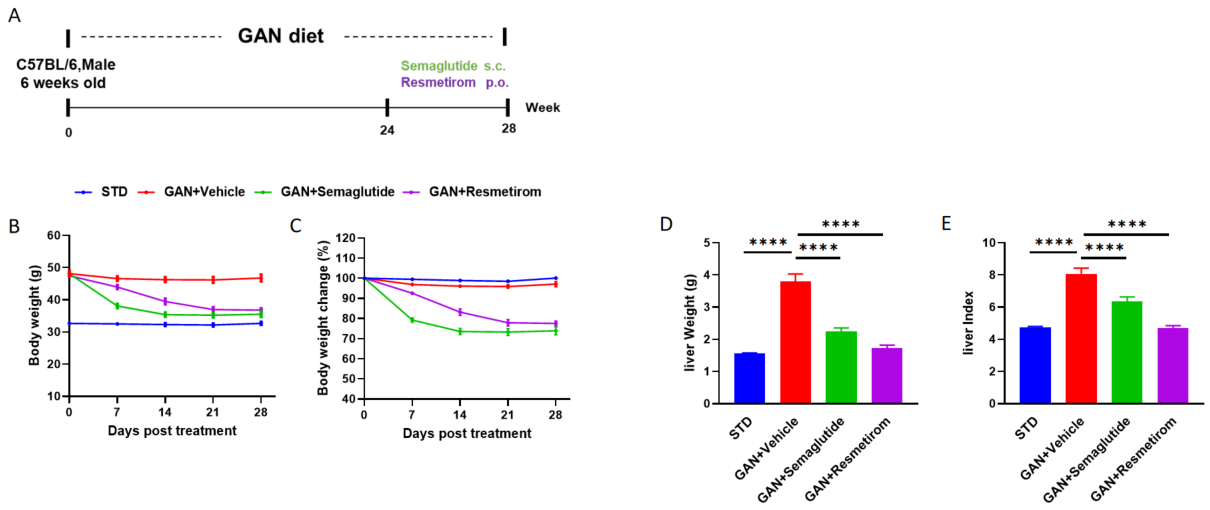
GAN 食餌誘発 NASH モデル(C57BL/6 マウス) A、GAN DIO-NASH マウスのモデル化と治療を示す試験デザイン。B-C、治療後の体重と体重変化率の比較。D-E、終了時の肝臓重量と肝臓指数の測定。各群 N = 9-10 匹のマウス。*p<0.05、**p<0.01、***p<0.001、****p<0.0001。
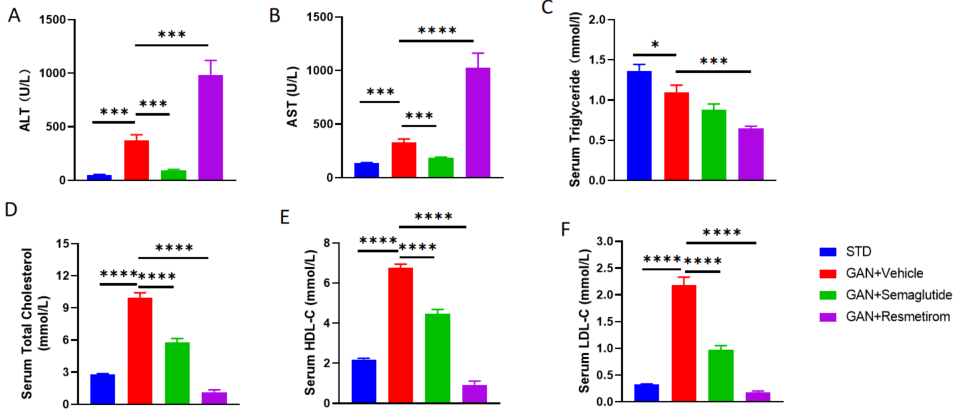
GAN 食餌誘発 NASH モデル(C57BL/6 マウス)A-B、試験終了時に、異なる群の ALT と AST のレベルを分析しました。C-F、終了時の異なる群の血清 TG、TC、HDL-C、LDL-C のレベルの測定。データは平均 ± SEM として表示されています。各群 N = 9-10 匹のマウス。*p<0.05、**p<0.01、***p<0.001、****p<0.0001。
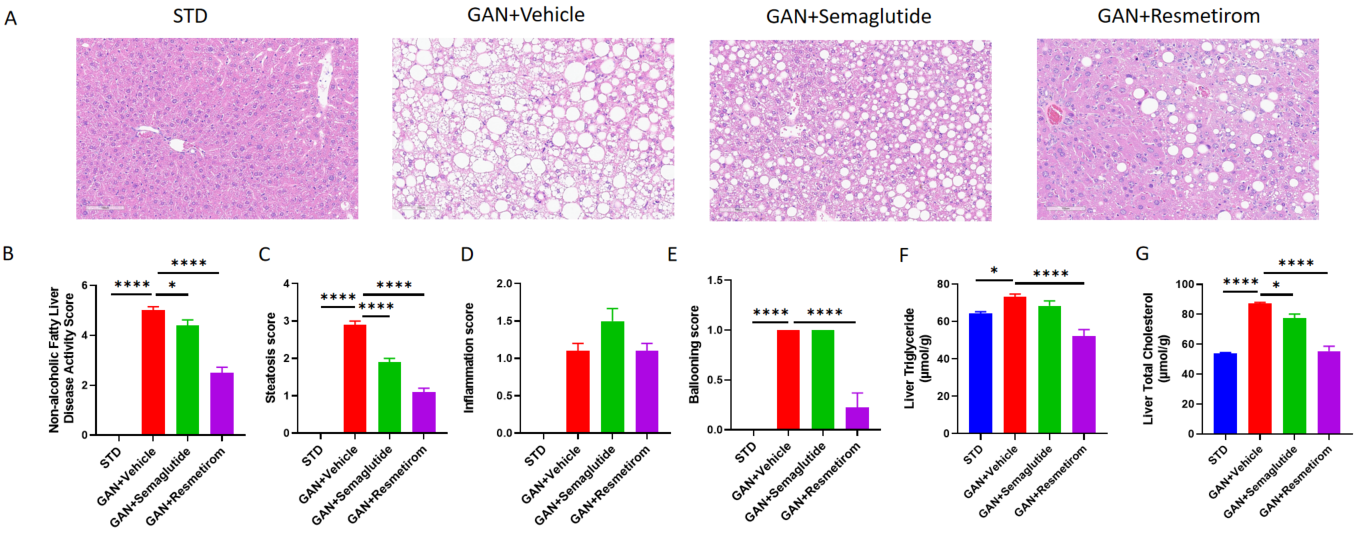
GAN DIO-NASH モデルにおけるSemaglutide と Resmetirom の肝臓への影響 A、H&E 染色の代表的な画像で NASH の程度を示す。B-E、NAFLD 活動スコア(NAS)、脂肪変性スコア、気球状変化スコア、炎症スコアの組織学的評価。F-G、試験終了時の TG と TC 含量。データは平均 ± SEM として表現されています。各群 N = 9-10 匹のマウス。*p<0.05、**p<0.01、***p<0.001。
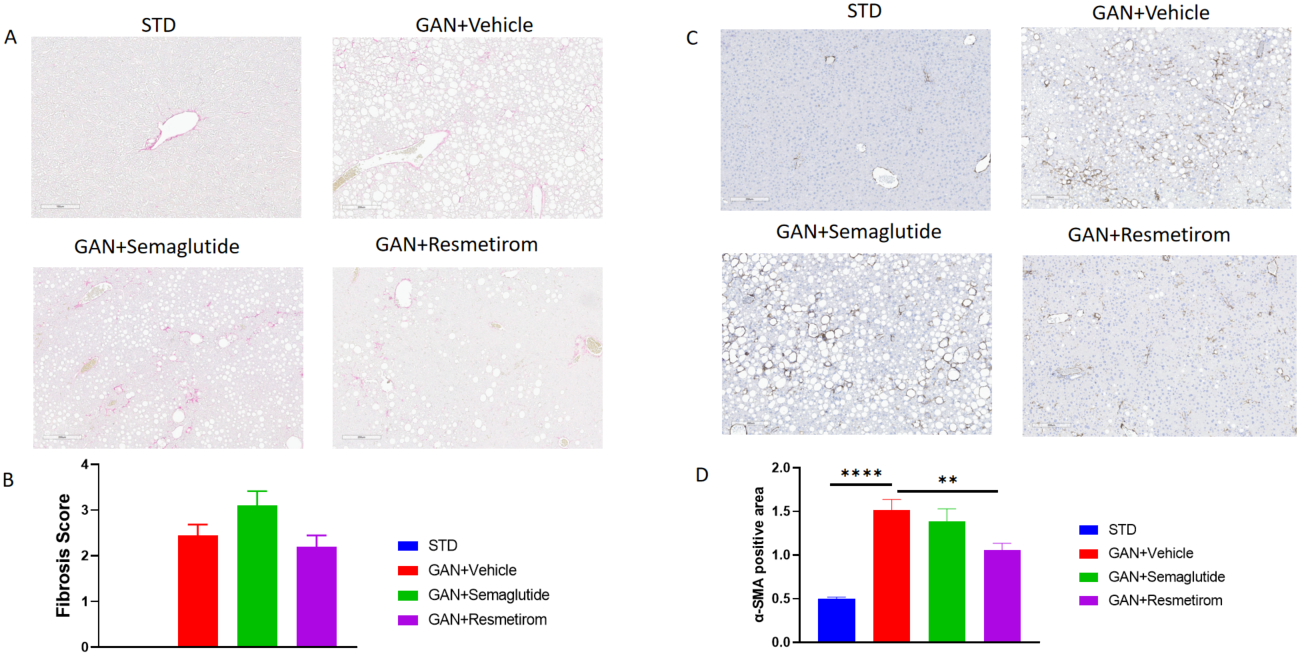
A、Sirius Red 染色の代表的な画像で肝線維症の程度を示します(スケールバー:200μm)。B、Sirius Red 染色に基づいて評価された肝線維症スコア。C、IHC 染色の代表的な画像で α-SMA の発現を示す(スケールバー:200μm)。D、α-SMA 発現の定量データ。データは平均 ± SEM として表現されています。各群 N = 9-10 匹のマウス。*p<0.05、**p<0.01、*p<0.001、****p<0.0001。
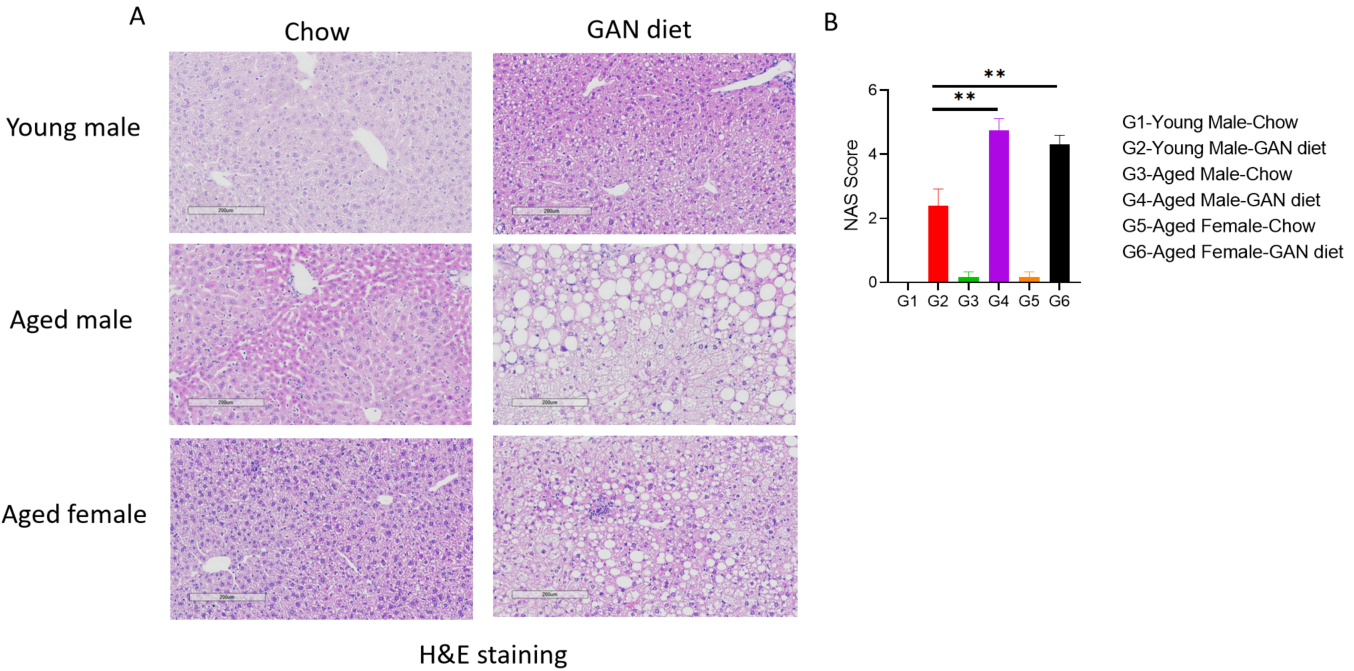
高齢マウスにおけるGubra-Amylin 食餌誘発 NASH A、誘発12 週間後の H&E 染色の代表的な画像。B、外部の専門病理医によって評価された NAFLD 活動スコア(NAS)。各群 N = 6-10 匹のマウス。データは平均 ± SEM として表示されています。:p<0.01。
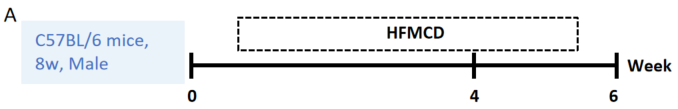
8 週齢の C57BL/6 雄マウスに、標準食(STD)または高脂肪メチオニン胆汁欠乏食を 4 週間または 6 週間与えました。
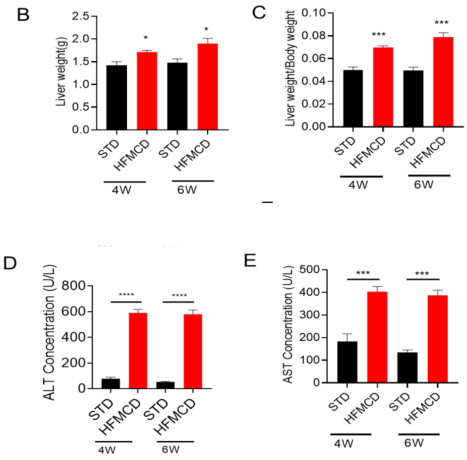
HFMCD 誘発性 NASH モデルの表現型解析 A、モデル化図。B-C、誘発後4 週間および 6 週間の肝臓重量および肝臓重量と体重の比率;n = 5 匹/群。D-E、HFMCD 誘発後の ALT および AST のレベル。データは平均 ± SEM として表示されています。*p<0.05、***p<0.001、****p<0.0001。

HFMCD誘発性 NASH マウスモデルの H&E と Sirius Red 染色解析 A、HFMCD 群の H&E 染色の代表的な画像で、肝脂肪変性と炎症の増加を示します。B、外部の病理専門医の評価によって、NAFLD 活動スコア(NAS)と、HFMCD 誘発後の NAS が有意に増加したことを示します。スケールバー:50μm。データは平均 ± SEM として表示されています。各群 N = 6 匹のマウス。*p<0.05、****p<0.0001。
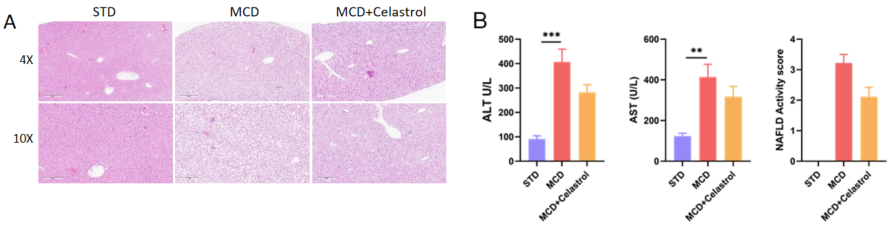
HFMCD 誘発 NASH マウスモデルにおける H&E 染色、肝機能および NAFLD 活性スコアの解析 A、Celastrol 投与後の H&E 染色の代表的な画像で、肝脂肪変性と炎症の減少を示します。B、MCD 誘発後の ALT/AST の変化。NAFLD 活性スコア(NAS)の統計データ。データは平均 ± SEM として表示されています。各群 N = 6 匹のマウス。**p<0.01、***p<0.001。
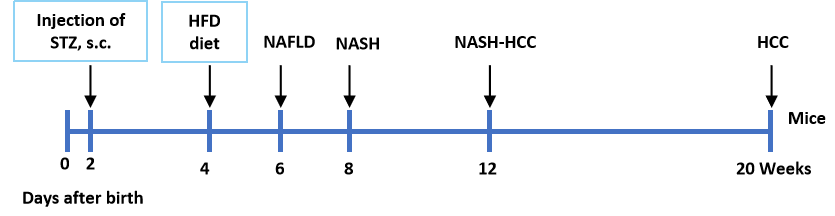
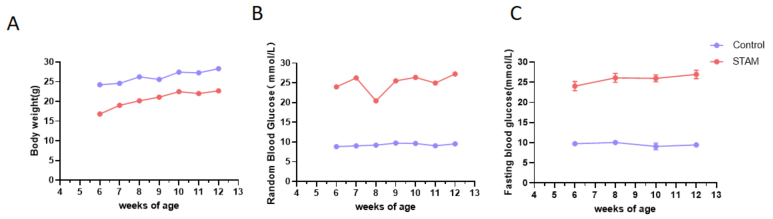
STAM モデルの特徴 新生児マウス(雄)の2日目に STZ を投与し、4 週齢から高脂肪食(HFD)を与えました。A-C、誘発後の体重および血糖の変化。各群 N = 8 匹のマウス。
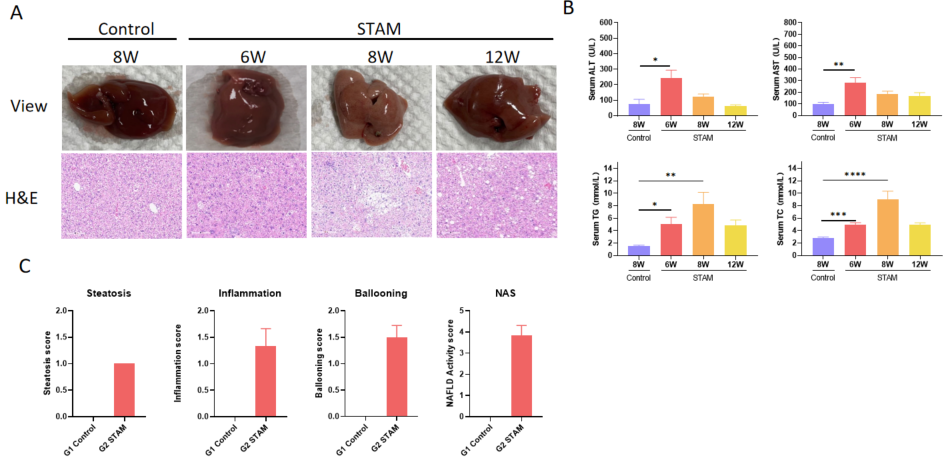
STAM モデルの特徴 A、誘発後6 週、8 週、12 週の H&E 染色の代表的な画像。B、STAM モデルの特徴を示す血液生化学結果。C、NAFLD 活動スコア。データは平均 ± SEM として表示されています。各群 N = 8 匹のマウス。*p<0.05、**p<0.01、***p<0.001、****p<0.0001。
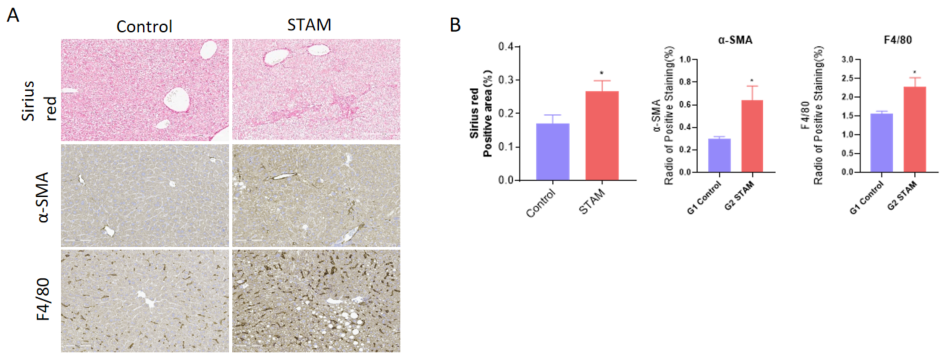
STAM モデルにおける線維化と炎症の解析 A、誘発後9 週間の Sirius Red と IHC 染色の代表的な画像。B、Sirius Red と IHC 染色の定量データ。データは平均 ± SEM として表示されています。各群 N = 8 匹のマウス。*p<0.05。
| GAN diet+CCL4 | GAN diet | HFMCD | STAM | |||
| Animal | C57BL/6 | C57BL/6 | C57BL/6 (Aged) | B-ob/ob | C57BL/6 | C57BL/6 (Neonatal) |
| Obesity | + | + | + | + | - | - |
| Dyslipidemia | + | + | + | + | Decreased TG and TC | + |
| Hepatomegaly | + | + | + | + | + | + |
| Liver enzymes | + | + | + | + | + | + |
| Steatosis | + | + | + | + | + | + |
| Inflammation | + | Mild | + | + | + | + |
| Fibrosis | + | Mild | Mild | Mild | + | + |
| Induction period (weeks) | 14 | 20-35 | 12-20 | 12-16 | 4-8 | 6-9 |
参考文献