このページで
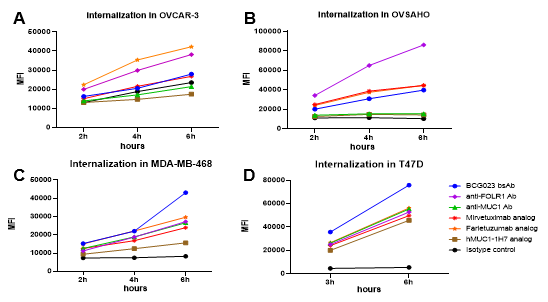
(A-D) 四つの哺乳類細胞株でのBCG023二重特異性抗体の内因性。内因性はpH感受性染料でFACSにより測定されました。BCG023二重特異性抗体は、ベンチマークに比べて優れた内因性活性を示し、MDA-MB-468 (C)およびT47D (D)腫瘍細胞株において親抗体に比べて強化された内因性を示しました。抗-FOLR1単クローン抗体は、すべての細胞株でベンチマークに対して強いまたは同等の活性を示しました。
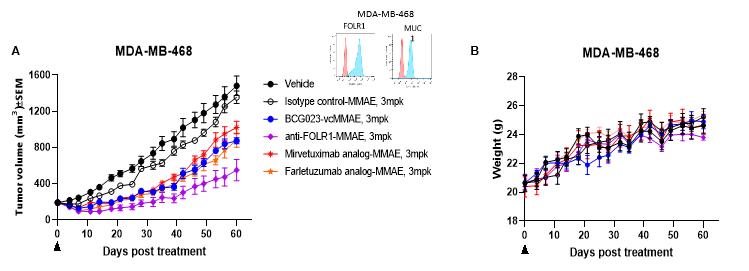
(A) TNBC MDA-MB-468異種移植モデルでのBCG023二重特異性ADCの効能研究。すべてのADCはvcMMAEと結合しており、DARは約4です。抗-FOLR1-MMAEは、2種類のFOLR1ベンチマークADCと比較して強い抗腫瘍効果を示し、BCG023-vcMMAEはFOLR1ベンチマークADCと同等の効果を示しました。実験期間中、小鼠の体重は減少しませんでした。(B)
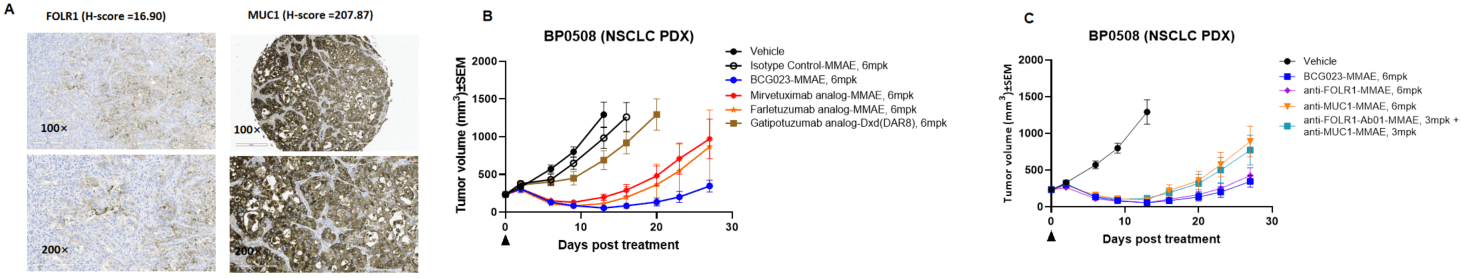
BCG023二重特異性ADCは、低FOLR1発現のNSCLC PDXモデルにおいて強力な抗腫瘍効果を示しました。
(A) PDXモデルにおけるFOLR1およびMUC1の発現。
(B, C) BCG023-vcMMAEの効能研究。すべてのADCは同じ薬物負荷(vcMMAE)を持ち、DARは約4ですが、Gatipotuzumab類似物-Dxd(DAR約8)を除きます。BCG023-MMAEは、PDXモデルでのベンチマークADCよりも効果的であり、親抗体MUC-1 ADC単独またはMUC-1およびFOLR1 ADCの併用よりも優れた効果を示しました。
葉酸受容体アルファ(FOLR1)は、卵巣癌、肺癌、乳癌などの上皮由来の悪性腫瘍に特異的に過剰発現しています。FOLR1をターゲットにした抗体薬物偶合物(ADC)治療は臨床試験で有望な結果を示していますが、低FOLR1発現の患者を含む大多数の患者は反応しないため、新たな治療戦略が必要であることを示唆しています。MUC1は、卵巣癌、乳癌、NSCLCをはじめとする他の癌においても過剰発現している別の腫瘍関連抗原です;卵巣PDX腫瘍の免疫組織化学(IHC)分析では、FOLR1とMUC1がこの癌タイプで高い発現を示すことが確認されています。
RenLiteおよびADCプラットフォームについてもっと学びましょう。