このページで
| EC50(ug/ml) | Clone A | Clone B | Clone C | Company A | Company B | Company C |
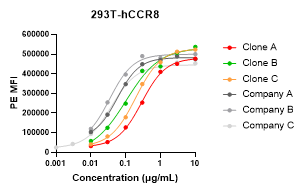
| 293T-hCCR8 | 0.287 | 0.104 | 0.194 | 0.058 | 0.035 | 0.039 |
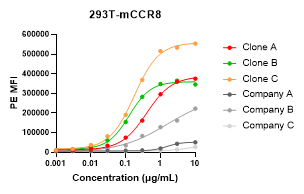
| 293T-mCCR8 | 0.400 | 0.127 | 0.177 | >10 | >10 | >10 |
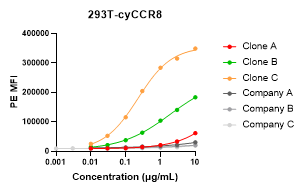
| 293T-cyCCR8 | >10 | >10 | 0.226 | >10 | >10 | >10 |
293T細胞にヒトCCR8(hCCR8)、マウスCCR8(mCCR8)またはサルCCR8(cyCCR8)をトランスフェクションし、FACSで抗体の結合を測定しました。会社A:Shionogi 10A11類似物;会社B:BMS 4A19類似物;会社C:Gilead 7B16類似物。
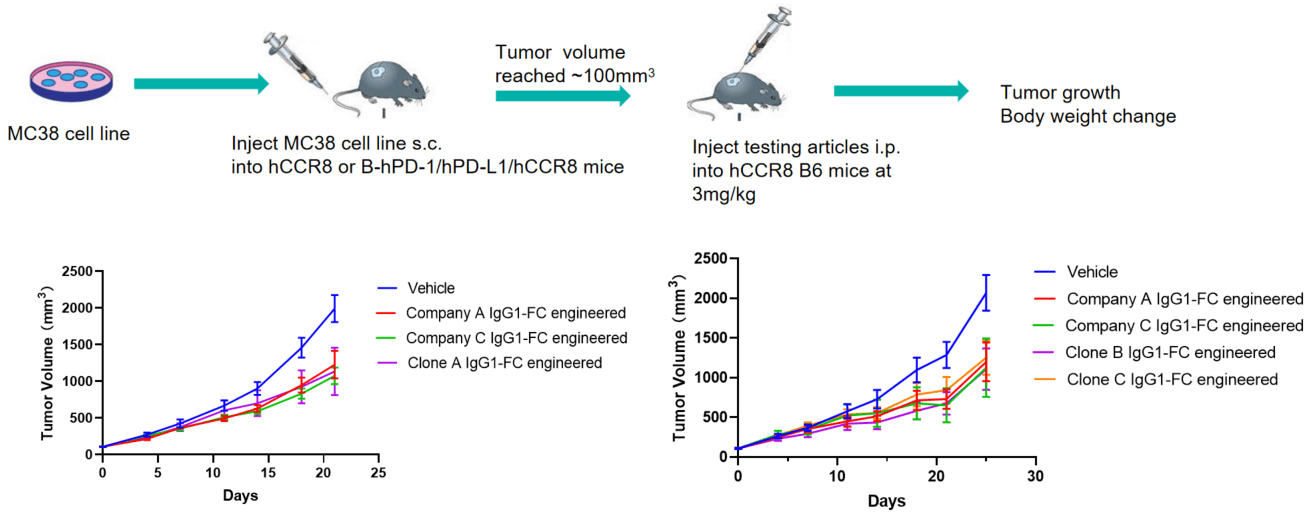
抗CCR8抗体は、結腸癌モデルでその腫瘍成長への影響をテストしました。約5 × 105のMC38細胞(マウス結腸癌細胞)をB-hCCR8マウスまたはB-hPD-1/hPD-L1/hCCR8マウスに皮下注射しました。マウスの腫瘍体積が約100mm3に達したとき、腫瘍体積に基づいてマウスをランダムに異なるグループに配置しました。その後、PBSまたは抗ヒトCCR8抗体を腹腔内(i.p.)注射し、腫瘍体積を監視しました。会社A:Shionogi 10A11類似物;会社B:BMS 4A19類似物;会社C:Gilead 7B16類似物。
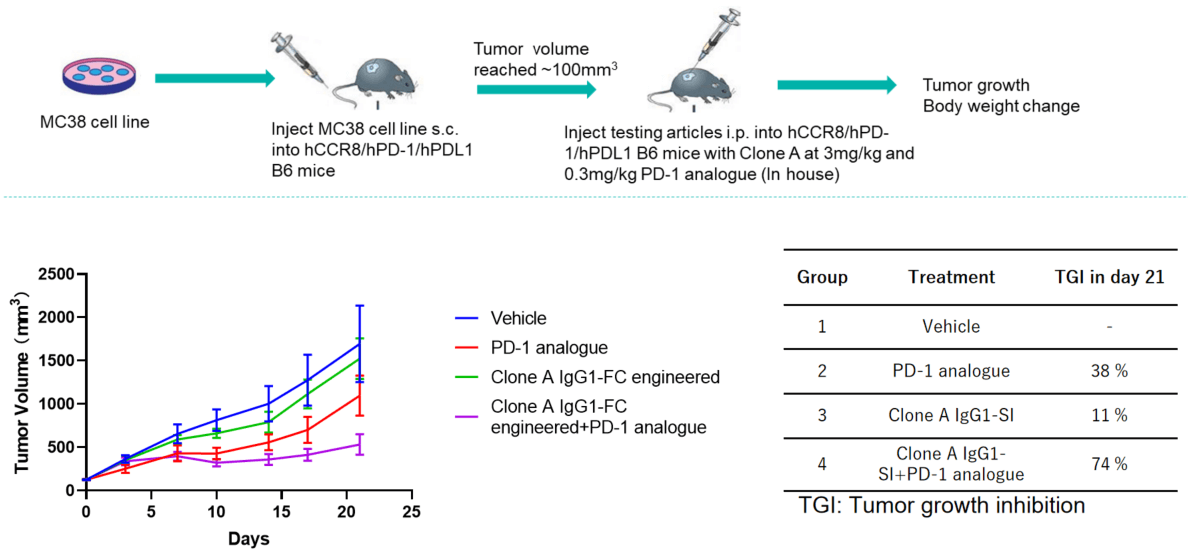
各B-hPD-1/hPD-L1/hCCR8マウスに5 × 105のMC38細胞(マウス結腸癌細胞)を皮下注射しました。腫瘍体積が約100-150mm3に達したとき、腫瘍体積に基づいてマウスをランダムに異なるグループに配置し(各グループ6匹)、その後PBS、0.3mg/kg Pembrolizumab類似物、3mg/kg Clone A、または0.3mg/kg Pembrolizumab類似物と3mg/kg Clone Aの組み合わせを腹腔内注射しました。抗体は毎週1日目と4日目に注射し、3週間で合計6回注射されました。腫瘍体積を監視しました。
免疫チェックポイント抑制療法(ICT)は、さまざまな種類の腫瘍に対して顕著な利益を示しています。しかし、かなりの数の患者はICTに対して良好な反応を示しません。ICTに対する耐性の一つの提案されたメカニズムは、大量の調節性T細胞(Tregs)が腫瘍に浸潤し、有効な抗腫瘍免疫の発展を妨げ、予後不良を引き起こすことです。CCR8はGタンパク質共役受容体(GPCR)であり、主に腫瘍Tregsで発現しています。
RenLiteおよびADCプラットフォームについて詳しく学ぶ。